题目内容
19.某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出.这一现象激发起同学们的探究欲望,生成的是什么气体?请你参与下列探究:【提出猜想】从物质组成元素的角度,放出的气体可能是SO2、O2、H2.
【查阅资料】SO2易溶于水,它能与NaOH反应,生成Na2SO3.
【方案设计】依据上述猜想,实验小组同学分别设计了探究方案
(1)甲同学认为是O2,则检验方法是用带火星的木条试验,看木条是否复燃.
(2)乙同学认为是SO2,则只需将放出的气体通入盛有NaOH溶液的洗气瓶中,称量通气前后洗气瓶的质量.写出SO2与NaOH反应的化学方程式SO2+2NaOH=Na2SO3+H2O.
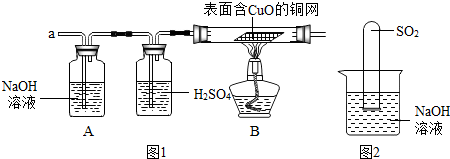
(3)实验小组同学合作设计了如图1组合实验方案,排除和验证猜想的气体.如果放出的是O2和H2,你认为方案中的安全隐患是B装置加热可能发生爆炸.
丙同学认为:为确保安全,实验前应先收集一试管气体,用拇指堵住试管口,管口向下移近火焰,若不发出尖锐的爆鸣声,方可采用上面的装置进行实验.
【实验探究】经丙同学确认安全后,小组同学首先对装置A进行称量,再将收集到的气体从a通入,过一会儿点燃B处酒精灯;一段时间后,发现表面含CuO的铜网由黑色变为光亮的红色:停止通气,再次称量装置A,发现质量无增减.
【探究结论】
(4)铁粉与硫酸铜溶液反应时,产生的气体是H2.
【拓展延伸】
(5)由上述实验可以推出,硫酸铜溶液中可能含有的物质是酸.
(6)不通过称量,如何判断S02与NaOH溶液发生了反应呢?有一同学设计了如图2所示的装置进行实验,发现试管内液面上升,就得出S02与NaOH溶液发生反应的结论.其他同学认为这一方案不严谨,理由是SO2易溶于水.
要得到科学严谨的结论,仍利用该装置,补做的实验是用SO2和水做一个对比试验.
分析 铁是一种活动性较强的金属,可以与酸反应产生氢气,产生的氢气具有可燃性和还原性,若不纯点燃或加热易爆炸,可以用来还原某些金属氧化物,铁还可以与硫酸铜溶液反应,置换出其中的铜;氧气能使带火星的木条复燃;二氧化硫是酸性气体,能与碱反应生成盐和水.
解答 解:
(1)氧气具有助燃性,更是带火星的木条复燃,所以本题答案为:用带火星的木条试验,看木条是否复燃;
(2)二氧化硫是酸性气体,可以与碱氢氧化钠反应生成亚硫酸钠和水,故本题答案为:SO2+2NaOH=Na2SO3+H2O,
(3)氢气具有可燃性,如若不纯,点燃或加热时易产生爆炸事故,所以使用前要注意验纯,一般采用小试管收集点燃的方法,不纯时能发出尖锐的爆鸣声,故本题答案为:实验时剩余气体B通过加热的试管易发生爆炸事故,堵住试管囗,靠近火焰点火,尖锐的爆鸣声;
(4)未发出爆鸣声,说明不含有氧气,称量NaOH溶液,发现质量无增减,说明不含二氧化硫,表面含CuO的铜网由黑色变为光亮的红色,说明氧化铜被还原为铜,故产生的气体为氢气,所以本题答案为:H2
(5)根据现象推断,产生的气体为氢气,而铁是与酸反应产生氢气,所以推断此硫酸铜溶液中含有酸性物质,故本题答案为:酸性.
(6)有一同学设计了如图2所示的装置进行实验,发现试管内液面上升,就得出S02与NaOH溶液发生反应的结论.其他同学认为这一方案不严谨,理由是SO2易溶于水;要得到科学严谨的结论,仍利用该装置,补做的实验是用SO2和水做一个对比试验.
答案:
(1)用带火星的木条试验,看木条是否复燃;
(2)SO2+2NaOH=Na2SO3+H2O;
(3)B装置加热可能发生爆炸; 尖锐的爆鸣声;
(4)H2;
(5)酸
(6)SO2易溶于水; 用SO2和水做一个对比试验.
点评 本题综合考查了金属的化学性质、氧气的检验、使用氢气的注意事项以及碱的部分性质,常见气体的鉴别主要有氧气、二氧化碳、氮气、氢气、空气等,选择鉴别方法时,要根据气体性质的差异.

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案| A. | 西达本胺是混合物 | |
| B. | 西达本胺有48个原子 | |
| C. | 西达本胺中碳元素和氢元素的质量比为22:19 | |
| D. | 西达本胺由碳、氢、氟、氮、氧五种元素组成 |
| A. | 盐酸 | B. | 纯碱 | C. | 干冰 | D. | 氢氧化钙 |
| A. | 用肥皂水鉴别硬水和软水 | |
| B. | 用水鉴别氢氧化钠固体和硝酸铵固体 | |
| C. | 用点燃闻气味的方法鉴别羊毛和合成纤维 | |
| D. | 用酚酞溶液鉴别碳酸钠溶液和氢氧化钠溶液 |
| A. |  添加酒精 | B. | 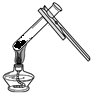 加热固体 | C. | 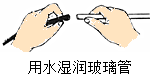 连接导管和胶管 | D. | 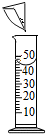 溶解固体 |