题目内容
9.小明在实验室用如图所示的流程图还原氧化铜,获取铜单质.求:(1)图中A气体为CO2.(填化学式)
(2)若实验室共有40g氧化铜,当其全部被还原后,得到的铜单质的质量.

分析 (1)根据焦炭在空气中充分燃烧生成二氧化碳,进行分析解答.
(2)一氧化碳还原氧化铜生成铜和二氧化碳,由参加反应的氧化铜的质量,根据反应的化学方程式列式计算出生成铜的质量即可.
解答 解:(1)焦炭在空气中充分燃烧生成二氧化碳,故图中A气体为二氧化碳,其化学式为:CO2.
(2)设生成铜的质量为x
CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2
80 64
40g x
$\frac{80}{64}=\frac{40g}{x}$ x=32g
故答案为:(1)CO2;(2)得到的铜单质的质量为32g.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.氧气和二氧化碳在性质上的相似点有( )
①都具有氧化性
②都具有还原性
③都易溶于水
④都能跟碳反应
⑤都是气体
⑥都是氧化物
⑦都不支持燃烧
⑧通常状况下密度都比空气大.
①都具有氧化性
②都具有还原性
③都易溶于水
④都能跟碳反应
⑤都是气体
⑥都是氧化物
⑦都不支持燃烧
⑧通常状况下密度都比空气大.
| A. | ②④⑤⑧ | B. | ①③④⑤⑥⑧ | C. | ①④⑤⑧ | D. | ①④⑤⑦⑧ |
17.下列说法正确的是( )
| A. | 4个H2O分子和1个H2SO4分子所含氧原子个数相等 | |
| B. | C24H38O4中碳、氧元素质量比为6:1 | |
| C. | 2gH2和32gO2充分反应后生成34gH2O | |
| D. | $\stackrel{+2}{Mg}$:“+2”表示每个镁离子带两个单位正电荷 |
1.甲、乙、丙、丁四个小组同学分别对实验室某无色废液的成分进行检测,向废液中滴入紫色石蕊溶液,溶液变蓝色,四组同学的分析结果如表.检测结果合理的组别是( )
| 检测小组 | 检测结果 |
| 甲组 | Na2SO4、HCl、BaCl2 |
| 乙组 | KCl、K2CO3、KOH |
| 丙组 | KCl、K2SO4、FeCl3、 |
| 丁组 | KCl、K2CO3、HCl |
| A. | 甲组 | B. | 乙组 | C. | 丙组 | D. | 丁组 |
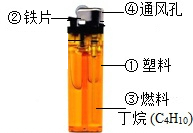 打火机给人们的生活带来了方便,如图为普通打火机的示意图,请根据如图回答下列问题:
打火机给人们的生活带来了方便,如图为普通打火机的示意图,请根据如图回答下列问题: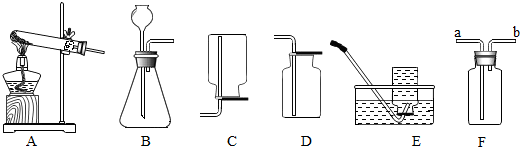
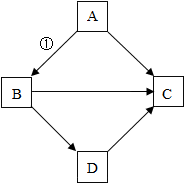 物质之间的相互转化是科学中的重要知识.某同学在复习物质性质时,绘制了如下框图.框图中“→”表示物质之间可以向箭头所指方向一步转化.根据框图,回答下列问题.
物质之间的相互转化是科学中的重要知识.某同学在复习物质性质时,绘制了如下框图.框图中“→”表示物质之间可以向箭头所指方向一步转化.根据框图,回答下列问题.