题目内容
9.我国海岸线曲折,海洋资源十分丰富.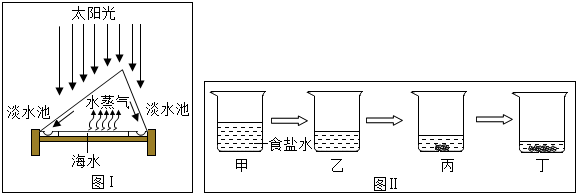
(1)如图Ⅰ所示,从海水中获得淡水的方法是蒸馏法,你认为该技术的优点是节约能源、减少成本.如下图Ⅱ所示,是恒温下模拟海水晒盐过程的示意图,与丙烧杯烧杯溶液的溶质质量分数一定相同的是丁(填序号,下同).
(2)从海水中提取金属镁,可按下图流程进行:
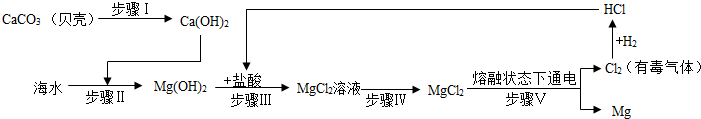
①写出步骤Ⅱ发生反应的化学方程式Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2.
②根据流程图,下列说法正确的是BC.
A.步骤Ⅰ通过一步反应即可实现
B.步骤Ⅱ、Ⅲ、Ⅳ的目的是从海水中提纯氧化镁
C.步骤Ⅲ发生了中和反应
D.步骤Ⅴ中化学能转化为电能
③该流程中采取的一种降低成本且减少污染的措施是将有毒的氯气转化为盐酸,既降低成本又减少污染.
(3)我国著名化学家侯德榜发明的“联合制碱法”主要工艺流程示意图如下:
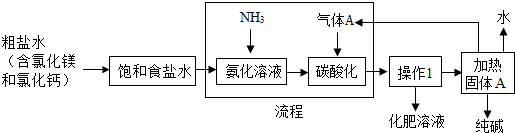
为了除去粗盐水中可溶性杂质,可加入下列物质,利用过滤等操作进行除杂,则加入下列三种物质的先后顺序为cab.
a.稍过量的Na2CO3溶液 b.适量的盐酸 c.稍过量的Ba(OH)2溶液②流程一,氨化溶液后,溶液的pH>7(填“>”、“<”或“═”),从而有利于吸收气体A,流程一反应的化学方程式为NH3+NaCl+H2O+CO2=NaHCO3+NH4Cl.
③加热固体A反应的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
分析 根据海水淡化的方法、海水制镁的方法和流程以及海水制碱的知识进行分析解答即可.
解答 解:(1)如图Ⅰ所示,从海水中获得淡水的方法是蒸馏法,使用该技术的优点是节约能源、减少成本.恒温下模拟海水晒盐过程的示意图,丙和丁都是饱和溶液,故与丙烧杯烧杯溶液的溶质质量分数一定相同的是丁,故填:蒸馏法;节约能源、减少成本;丁.
(2)①氢氧化钙能与氯化镁反应生成氢氧化镁沉淀和氯化钙,故填:Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2.
②A.步骤Ⅰ通过碳酸钙高温分解生成氧化钙和水、氧化钙能与水反应生成氢氧化钙,不能通过一步反应实现,错误;
B.步骤Ⅱ、Ⅲ、Ⅳ的目的是从海水中提纯氧化镁,正确;
C.步骤Ⅲ是氢氧化镁与盐酸反应,发生的是中和反应,正确;
D.步骤Ⅴ中是电能转化为化学能,错误;
故填:BC;
③该流程中采取的一种降低成本且减少污染的措施是将有毒的氯气转化为盐酸,既降低成本又减少污染,故填:将有毒的氯气转化为盐酸,既降低成本又减少污染.
(3为了除去粗盐水中可溶性杂质,可加入稍过量的Ba(OH)2溶液、稍过量的Na2CO3溶液、适量的盐酸,利用过滤等操作进行除杂,故加入下列三种物质的先后顺序为 cab,故填:cba.
②流程一,氨化溶液后,溶液呈碱性,溶液的pH大于7,从而有利于吸收气体A,流程一反应的化学方程式为NH3+NaCl+H2O+CO2=NaHCO3+NH4Cl,故填:NH3+NaCl+H2O+CO2=NaHCO3+NH4Cl.
③加热固体碳酸氢钠分解生成碳酸钠、水和二氧化碳,故填:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
点评 本题考查的是海水的综合利用的知识,完成此题,可以依据已有的知识进行.

 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案| A. | NH4HCO3$\frac{\underline{\;△\;}}{\;}$NH3↑+CO2↑+H2O | B. | Na2CO3+SiO2$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑ | ||
| C. | CaCO3+CO2+H2O=Ca(HCO3)2 | D. | 2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C |
| A. | 溶液质量分数 | B. | 溶液的pH | ||
| C. | 氢氧化钠的溶解度 | D. | 最多能吸收二氧化碳的质量 |
| A. | KNO3=K++NO3- | B. | NaCl=Na++Cl- | C. | H2SO4=2H++SO42- | D. | NaOH=Na++OH- |
| A. | 钙原子 | B. | 钙元素 | C. | 钙分子 | D. | 钙单质 |

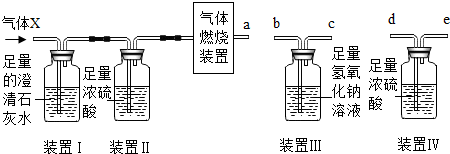
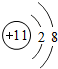 ,Y原子
,Y原子 ,Z元素的离子
,Z元素的离子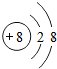 .若将0.62克X2Z放入18.2克水中得A溶液,则溶液中溶质的质量分数为4.3%,pH值>7(填“>”,“<”,“=”).
.若将0.62克X2Z放入18.2克水中得A溶液,则溶液中溶质的质量分数为4.3%,pH值>7(填“>”,“<”,“=”).