题目内容
9.现有NaNO3和Na2CO3的混合物20g,为了除掉其中的Na2CO3,配制NaNO3溶液.小明同学将该混合物放入一定量的水中配制成60g溶液,再向其中加入50gCa(NO3)2溶液,恰好完全反应,生成了CaCO3沉淀,过滤后得到100g溶液,求:(1)生成了CaCO3沉淀的质量;
(2)所得溶液中溶质的质量分数.
分析 碳酸钠和硝酸钙反应生成碳酸钙沉淀和硝酸钠,反应前后的质量差即为反应生成碳酸钙的质量,根据碳酸钙的质量可以计算碳酸钠和反应生成的硝酸钠的质量,进一步可以计算所得溶液中溶质的质量分数.
解答 解(1)生成CaCO3沉淀的质量为:(60g+50g)-100g=10g,
答:生成了10g碳酸钙沉淀.
(2)设混合物中Na2CO3的质量为x,生成NaNO3的质量为y,
Na2CO3+Ca(NO3)2=CaCO3↓+2NaNO3,
106 100 170
x 10g y
$\frac{106}{x}$=$\frac{100}{10g}$=$\frac{170}{y}$,
x=10.6g,y=17g,
所得溶液中溶质的质量为:20g-10.6g+17g=26.4g,
所得溶液中溶质的质量分数为:$\frac{26.4g}{100g}$×100%=26.4%,
答:所得溶液中溶质的质量分数为26.4%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
20.下列反应发生后,固体质量增加的是( )
| A. | 铁丝在纯氧中剧烈燃烧 | B. | 加热高锰酸钾制取氧气 | ||
| C. | 氢气在加热条件下还原氧化铜 | D. | 将锌片插入稀硫酸中 |
14.建立微观和宏观之间的联系是一种科学的思维方式,下列叙述错误的是( )
| A. | 温度升高使原子之间的间隔变大,因此夏天钢轨之间的缝隙变小 | |
| B. | 石墨和金刚石的物理性质存在差异,因为构成它们的碳原子排列不同 | |
| C. | H2SO4、H2O、H2CO3三种物质中均含有氢分子 | |
| D. | 电解水生成氢气和氧气,是因为分子在化学变化中可以再分 |
1.某金属加工厂生产过程中的废液含有少量硝酸银和硝酸铜,为回收利用资源和防止污染,该厂向废液中加入一定量的铁粉,反应停止后过滤,向滤出的固体中加入少量稀盐酸,无气体产生.则下列有关说法中,正确的是( )
| A. | 滤出的固体中一定含有银,可能含有铁和铜 | |
| B. | 滤出的固体中一定含有银和铜,一定不含铁 | |
| C. | 滤液中一定有硝酸亚铁,一定没有硝酸银和硝酸铜 | |
| D. | 滤液中一定有硝酸亚铁,可能有硝酸银和硝酸铜 |
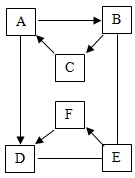 有A-F六种物质,已知A、B、C三种固体含有同种金属元素,A是大理石、石灰石的主要成分,B是一种氧化物能与E反应放出大量的热,D、E、F含有同种非金属元素,E通常状况下为液体,D、F通常状况下为气体,且F为单质.它们的转化关系如图(部分产物已略去).温馨提示:图中“→”表示箭尾的物质可转化为箭头的物质;“-”表示两端的物质能发生化学反应.
有A-F六种物质,已知A、B、C三种固体含有同种金属元素,A是大理石、石灰石的主要成分,B是一种氧化物能与E反应放出大量的热,D、E、F含有同种非金属元素,E通常状况下为液体,D、F通常状况下为气体,且F为单质.它们的转化关系如图(部分产物已略去).温馨提示:图中“→”表示箭尾的物质可转化为箭头的物质;“-”表示两端的物质能发生化学反应. 某化学小组在课外活动时按如图所示组装好仪器,在甲试管中装入碳酸钙,乙试管装入紫色石蕊溶液.
某化学小组在课外活动时按如图所示组装好仪器,在甲试管中装入碳酸钙,乙试管装入紫色石蕊溶液.