题目内容
3.氯气(Cl2)是黄绿色气体,氯气溶于水部分以Cl2分子存在于溶液中,部分与水反应Cl2+H2O=HCl+HClO.产物中,次氯酸HClO是一种弱酸.氯气溶于水所得溶液称为氯水.把品红试纸(染有品红颜料的滤纸)放入氯水中,品红试纸褪色.下图是实验室制取氯气的成套装置图,请填空: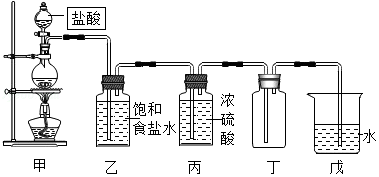
(1)从反应物的状态和反应条件看,装置甲属于①固液加热型气体发生装置.
(2)氯气在装置丁中被收集,其收集方法为②向上排空气法,装置戊中可得到氯水
(3)晓红对“氯水使品红试纸褪色”产生兴趣,她所在的学习小组进行了如下探究,请你一起来完成:
【提出问题】氯水中的什么成分使品红试纸褪色?
【猜 想】猜想1:氯水中的水使品红试纸褪色;猜想2:氯水中的Cl2使品红试纸褪色;
猜想3:氯水中的盐酸使品红试纸褪色;猜想4:氯水中的HClO(填化学式)使品红试纸褪色.
【实验探究】
| 实验操作 | 实验现象 | 结论 |
| ①把品红试纸放入水中 | 品红试纸不褪色 | 猜想1不成立 |
| ②把品红试纸放入干燥的氯气中 | 试纸不褪色 | 猜想2不成立 |
| ③品红试纸放入稀盐酸中 | 试纸不褪色 | 猜想3不成立 |
【反 思】向氯水中滴加几滴紫色石蕊试液,会观察到的现象是紫色石蕊试液先变红色,后颜色褪去,变成无色溶液.
分析 (1)实验室制取气体的发生装置应根据反应物的状态和反应发生的条件来确定,一般分为两种:①固体与固体反应生成气体,反应需要加热,简称“固固加热型”;②固体与液体反应生成气体,反应不需要加热,简称“固液不加热型”;
(2)根据收集气体的装置可以判断收集气体的方法;
(3)能使品红试纸褪色的物质可能是氯水中的水,或氯水中的Cl2,或氯水中的盐酸,或氯水中的HClO;
氯水显酸性,能使石蕊试液变红色,同时氯水能使石蕊试液褪色.
解答 解:(1)从反应物的状态和反应条件看,装置甲属于固液加热型气体发生装置.
故填:固液加热.
(2)氯气在装置丁中被收集,其收集方法为向上排空气法.
故填:向上排空气法.
(3)【猜想】
猜想1:氯水中的水使品红试纸褪色;
猜想2:氯水中的Cl2使品红试纸褪色;
猜想3:氯水中的盐酸使品红试纸褪色;
猜想4:氯水中的HClO使品红试纸褪色.
故填:HClO.
【实验探究】
①把品红试纸放入水中,品红试纸不褪色,猜想1不成立;
②把品红试纸放入干燥的氯气中,试纸不褪色,猜想2不成立;
③把品红试纸放入稀盐酸中,试纸不褪色,猜想3不成立.
故填:品红试纸不褪色;把品红试纸放入稀盐酸中.
【反思】
向氯水中滴加几滴紫色石蕊试液时,显酸性的溶液先使石蕊试液变红色,后使石蕊试液褪色,变成无色溶液,因此会观察到的现象是紫色石蕊试液先变红色,后颜色褪去,变成无色溶液.
故填:紫色石蕊试液先变红色,后颜色褪去,变成无色溶液.
答案:
(1)固液加热;
(2)向上排空气法;
(3)HClO;
【实验探究】①紫色石蕊试液先变红色,③品红试纸放入稀盐酸中
【反 思】紫色石蕊试液先变红色,后颜色褪去,变成无色溶液.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

| 执行标准:GB1413-99 主要成分:碳酸钙 含钙量:每片含钙0.75g 每瓶50片,重 40g (中外合资xx公司出品) |
(2)为测定其真实的含钙量,小东每次取10片钙片放入已称量的含足量盐酸的烧杯中,发生的化学反应是:CaCO3+2HCl=CaCl2+H2O+CO2↑,充分反应后再称取烧杯和剩余物的总质量.小东做了三次实验,数据如下:
| 物质的质量 | 第一次 | 第二次 | 第三次 | 平均值 |
| 反应前:烧杯+盐酸 | 22g | 22g | 22g | 22g |
| 10片钙片 | 8g | 8g | 8g | 8g |
| 反应后:烧杯十剩余物 | 26.7g | 26.5g | 26.9g | 26.7g |
| A. | 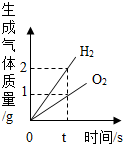 电解水 电解水 | |
| B. | 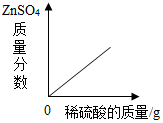 向一定量锌粒中加入过量稀硫酸 向一定量锌粒中加入过量稀硫酸 | |
| C. | 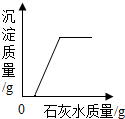 向一定量氢氧化钠和碳酸钠的混合溶液中加入过量的石灰水 向一定量氢氧化钠和碳酸钠的混合溶液中加入过量的石灰水 | |
| D. | 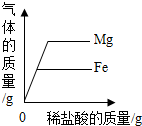 分别向等质量的镁和铁中滴入溶质质量分数相同的稀盐酸至过量 分别向等质量的镁和铁中滴入溶质质量分数相同的稀盐酸至过量 |
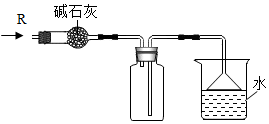 实验室可用如图所示装置干燥、收集气体R,并吸收多余的R,则R可能是( )
实验室可用如图所示装置干燥、收集气体R,并吸收多余的R,则R可能是( )| A. | CH4 | B. | CO2 | C. | Cl2 | D. | NH3 |
| A. | NO2 | B. | N2O4 | C. | CH4 | D. | N2O3 |
| A. | 法国化学家拉瓦锡研究了空气的成分,并得出氧气约占空气总体积$\frac{4}{5}$的结论 | |
| B. | 空气是由氮气、氧气、稀有气体、二氧化碳等物质组成的混合物 | |
| C. | 稀有气体都没有颜色、没有气味,在通电时能发出不同颜色的光 | |
| D. | 氮气是制造硝酸和氮肥的重要原料 |

 某同学用如图装置,利用碳酸饮料(如雪碧)中溶解的二氧化碳气体进行下列实验,请回答问题:
某同学用如图装置,利用碳酸饮料(如雪碧)中溶解的二氧化碳气体进行下列实验,请回答问题: