题目内容
杨雪松老师在实验室制取二氧化碳,他先将稀盐酸及烧杯的总质量称量是100g,然后加入10g大理石充分反应后称得总质量为107.8g.求:
(1)生成的二氧化碳的质量.
(2)大理石中碳酸钙的质量分数.
(1)生成的二氧化碳的质量.
(2)大理石中碳酸钙的质量分数.
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:(1)反应后剩余物的总质量比反应前的减少,根据质量守恒定律知,减少的质量就是生成二氧化碳的质量;
(2)由二氧化碳的质量根据碳酸钙与盐酸反应的化学方程式可以计算出大理石中碳酸钙的质量分数.
(2)由二氧化碳的质量根据碳酸钙与盐酸反应的化学方程式可以计算出大理石中碳酸钙的质量分数.
解答:解:(1)产生二氧化碳的质量为:100g+10g-107.8g=2.2g;
(2)设该大理石中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 2.2g
=
x=5g
大理石中碳酸钙的质量分数:
×100%=50%.
答:(1)产生二氧化碳的质量为2.2g;
(2)大理石中碳酸钙的质量分数为50%.
(2)设该大理石中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 2.2g
| 100 |
| 44 |
| x |
| 2.2g |
x=5g
大理石中碳酸钙的质量分数:
| 5g |
| 10g |
答:(1)产生二氧化碳的质量为2.2g;
(2)大理石中碳酸钙的质量分数为50%.
点评:本题主要考查质量守恒定律和含杂质物质的化学方程式计算,难度较大.

练习册系列答案
相关题目
小明阅读《科学画报》后,对抽烟的爸爸说:“吸烟有害健康,我和妈妈都在被动吸烟”.小明这样说的主要原因是( )
| A、分子很小 |
| B、分子间有间隙 |
| C、分子处于不停运动之中 |
| D、分子间有作用力 |
下列各组物质中,带点的同种元素的化合价相同的是( )
A、Ca3(
| ||||
B、Na
| ||||
C、K2
| ||||
D、
|
下列实验现象描述正确的是( )
| A、镁条在空气中燃烧,发出耀眼白光,产生白烟,生成黑色固体 |
| B、电解水时正极产生的气体比负极产生的少 |
| C、细铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁 |
| D、木炭在氧气中燃烧,发出白光,生成黑色固体 |
下列变化属于物理变化的是( )
| A、石油分馏制得汽油、柴油等物质 |
| B、石油液化气燃烧 |
| C、煤隔绝空气加热得到焦炭、煤焦油、煤气等 |
| D、秸杆、杂草发酵产生甲烷 |
下列说法中正确的是( )
| A、催化剂在化学反应前后质量和化学性质没有变化,但物理性质可能有变化 |
| B、氧气的化学性质很活泼,在常温下能与所有物质发生化学反应 |
| C、氧气能与许多物质发生反应,氧气具有可燃性 |
| D、没有二氧化锰作催化剂,过氧化氢溶液就不会产生氧气 |
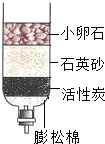 水是一种宝贵的自然资源.今春我国长江中下游地区发生了大面积干早,使工农业生产和居民生活受到了严重影响
水是一种宝贵的自然资源.今春我国长江中下游地区发生了大面积干早,使工农业生产和居民生活受到了严重影响