题目内容
5.元素周期表是化学学习和研究的重要工具,如图是其中一部分.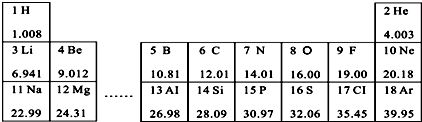
(1)从表中查出氖(Ne)元素的相对原子质量为20.18;
(2)13~18号元素中属于金属的有Al(填元素符号);
(3)表中不同种元素最本质的区别是A;
A.质子数不同 B.中子数不同 C.相对原子质量不同
(4)仅由l、7、8号元素组成的一种盐的化学式为NH4NO3.
分析 (1)根据元素周期表的信息来分析;
(2)依据13-18号元素的名称进行判断;
(3)根据不同种元素最本质的区别是质子数不同,进行解答;
(4)根据化学式的写法解答.
解答 解:(1)由元素周期表的信息可知,氖元素的相对原子质量为20.18;故填:20.18;
(2)根据化学元素汉字名称的偏旁可辨别元素的种类,通过归纳,金属元素名称一般有“钅”字旁,13~18号元素中属于金属的有Al;故填:Al;
(3)元素是具有相同核电荷数(即核内质子数)的一类原子的总称,不同种元素之间的本质区别是质子数不同,各选项中不同种元素最本质的区别是质子数不同;
故填:A;
(4)1号是氢元素,7号是氮元素,8号是氧元素,由1、7、8号元素组成的一种盐为硝酸铵,化学式为NH4NO3;故填:NH4NO3
点评 本题考查学生熟练掌握应用元素周期表所提供的信息进行分析解题的能力,属基础性知识考查题.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案
相关题目
20.如表有关物质除杂、分离、区分所用的试剂或方法都正确的( )
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 除去NaCl溶液中少量Na2CO3 | 适量澄清石灰水、过滤 |
| B | 除去二氧化碳中混有的水蒸气 | 通入装有生石灰的干燥管 |
| C | 从高锰酸钾制氧气的残余物中分离出MnO2 | 加水溶解、过滤、洗涤、干燥 |
| D | 区分失去标签的稀盐酸和稀硫酸 | 紫色石蕊溶液或铁粉 |
| A. | A | B. | B | C. | C | D. | D |
5.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格)
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH═Na2SO4 +2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么?
【假设猜想】针对疑问,大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是猜想四,理由是H2SO4和NaOH在溶液中不能共存.
【实验探究】
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有氢氧化钠.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、Na2CO3溶液、BaCl2溶液,进行如下三个方案的探究.
【得出结论】通过探究,全班同学一致确定猜想二是正确的.
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出(2)中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
①实验操作中的错误是pH试纸浸入溶液中.
②实验方案中也有一个是错误的,错误的原因是Na2SO4与BaCl2反应也会生成白色沉淀,不能证明一定有H2SO4存在.
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH═Na2SO4 +2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么?
【假设猜想】针对疑问,大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是猜想四,理由是H2SO4和NaOH在溶液中不能共存.
【实验探究】
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有氢氧化钠.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、Na2CO3溶液、BaCl2溶液,进行如下三个方案的探究.
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 |  |  |  |
| 实验现象 | 试纸变色,对比标准比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出(2)中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
①实验操作中的错误是pH试纸浸入溶液中.
②实验方案中也有一个是错误的,错误的原因是Na2SO4与BaCl2反应也会生成白色沉淀,不能证明一定有H2SO4存在.
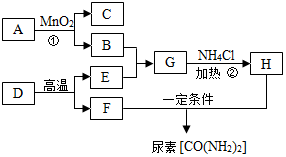 如图表示某些物质间转化关系.A、B为组成元素相同的无色液体,D是大理石的主要成分,C、F、H为气体,且H有刺激性气味.
如图表示某些物质间转化关系.A、B为组成元素相同的无色液体,D是大理石的主要成分,C、F、H为气体,且H有刺激性气味.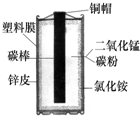 小芳从废干电池中回收有关物质并进行探究,请你参与研究.
小芳从废干电池中回收有关物质并进行探究,请你参与研究.