题目内容
某活泼金属R的化合价只有+1价,取该金属4.6克与147.6克的稀硫酸恰好完全反应,得到不饱和溶液的质量为
152克.
(1)R与稀硫酸反应的化学方方程式为 .
(2)金属R的相对原子质量为 .
(3)通过计算回答:所得不饱和溶液溶质的质量分数为多少?
152克.
(1)R与稀硫酸反应的化学方方程式为
(2)金属R的相对原子质量为
(3)通过计算回答:所得不饱和溶液溶质的质量分数为多少?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算,书写化学方程式、文字表达式、电离方程式
专题:溶质质量分数与化学方程式相结合的计算
分析:依据R的化合价利用该金属和硫酸的反应规律书写出两者反应的方程式,据此对相关问题进行分析解答;
解答:解:(1)金属与酸反应会生成盐和氢气,其方程式为2R+H2SO4═R2SO4+H2↑;
(2)依据质量守恒定律可知生成的氢气的质量是:4.6g+147.6g-152g=0.2g
设R的相对原子质量是x 生成的R2SO4质量是y;
2R+H2SO4═R2SO4+H2↑
2x 2x+96 2
5.6g y 0.2
=
=
x=28 y=15.2g
则所得溶液的溶质质量分数为
×100%=10%
故答案为:(1)2R+H2SO4═R2SO4+H2↑;(2)28;(3)所得不饱和溶液溶质的质量分数为10%.
(2)依据质量守恒定律可知生成的氢气的质量是:4.6g+147.6g-152g=0.2g
设R的相对原子质量是x 生成的R2SO4质量是y;
2R+H2SO4═R2SO4+H2↑
2x 2x+96 2
5.6g y 0.2
| 2x |
| 5.6g |
| 2x+96 |
| y |
| 2 |
| 0.2g |
x=28 y=15.2g
则所得溶液的溶质质量分数为
| 15.2g |
| 152g |
故答案为:(1)2R+H2SO4═R2SO4+H2↑;(2)28;(3)所得不饱和溶液溶质的质量分数为10%.
点评:此题是依据化学方程式考查的计算题,解题的关键是能够对相关方程式的书写和基本的化学计算;

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
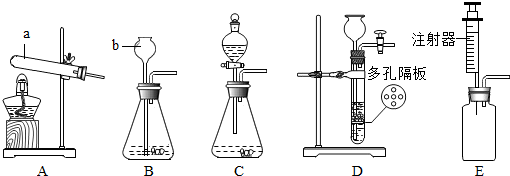
加热50mL液体时,所需的仪器是( )
①试管 ②烧杯 ③酒精灯 ④试管夹 ⑤石棉网 ⑥铁架台.
①试管 ②烧杯 ③酒精灯 ④试管夹 ⑤石棉网 ⑥铁架台.
| A、①③⑤ | B、②③⑤⑥ |
| C、②③④⑥ | D、①③⑤⑥ |
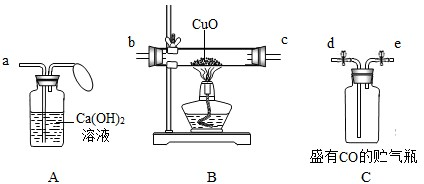 用如图提供的装置和试剂,组装一套用一氧化碳使氧化铜还原成铜的实验装置,并回答问题.
用如图提供的装置和试剂,组装一套用一氧化碳使氧化铜还原成铜的实验装置,并回答问题.