题目内容
6. 在实验室用如图所示装置进行CO和CO2的分离和干燥.现只有稀盐酸、浓硫酸、
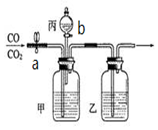
在实验室用如图所示装置进行CO和CO2的分离和干燥.现只有稀盐酸、浓硫酸、氢氧化钠溶液,按要求填写下列空白(如图所示装置中a是弹簧夹,b是分液漏斗活塞)
(1)①先关闭b打开a;②通入混合气体,则乙中排出CO气体.
(2)若获得另一种气体,混合气体通入完毕后,应继续的操作为关闭a打开b,丙中盛放的溶液为稀盐酸,此刻甲中反应的化学方程式:Na2CO3+2HCl=2NaCl+H2O+CO2↑.
分析 (1)CO与氢氧化钠溶液不反应,CO2氢氧化钠可反应生成碳酸钠,所以先出来的是一氧化碳;(2)碳酸钠和盐酸反应可生成二氧化碳,浓硫酸具有吸水性,可干燥气体,且气体从溶液中出来时要带来部分水蒸气,故乙瓶中盛放的是浓硫酸,据此分析实验步骤,并依据反应原理书写方程式.
解答 解:(1)要将CO和CO2分离,可在甲中装有NaOH溶液,用来吸收CO2,先分离出被乙中浓硫酸干燥过的纯净的CO,所以关闭b,打开a,混合气体进入甲装置,CO与氢氧化钠溶液不反应,可分离出 被乙中浓硫酸干燥过的纯净的CO;
(2)二氧化碳与氢氧化钠溶液在甲中反应生成碳酸钠,要得到CO2,可在丙中盛放稀盐酸,然后关闭活塞a,打开b,从丙处加入稀盐酸,稀盐酸与碳酸钠可反应生成氯化钠、水和二氧化碳,又可分离出被乙中浓硫酸干燥过的纯净的CO2;反应的化学方程式为 Na2CO3+2HCl=2NaCl+H2O+CO2↑;
故答案为:
(1)CO(2)关闭a打开b;稀盐酸,Na2CO3+2HCl=2NaCl+H2O+CO2↑
点评 此题考查了设计实验分离CO与CO2,掌握气体的性质是解答的关键,可先利用气体的性质加入试剂除掉一种物质,而后再把吸收后的物质与其他物质反应制取出开始除掉的气体.

练习册系列答案
相关题目
12.下列事实不能用同一原理进行解释的是( )
| A. | C和H2都能跟灼热的CuO反应 | |
| B. | 在滴有酚酞的NaOH溶液中加盐酸或活性炭都褪色 | |
| C. | 碳酸饮料和白醋都能使紫色石蕊试液变红 | |
| D. | 实验室收集CO2和为O2都能用向上排空气法 |
1.下列化学用语表达正确的是( )
| A. | 五个氢原子:5H | B. | 水中氧元素的化合价:H2$\stackrel{-2}{O}$ | ||
| C. | 两个钙离子:2Ca+2 | D. | 四个氨分子:4NH4 |
18.下列实验操作错误的是( )
| A. | 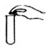 加入固体 | B. | 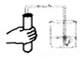 检查气密性 | C. | 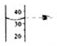 读液体体积 | D. | 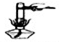 加热反应物 |
15.下列所示的实验操作中,不正确的是( )
| A. | 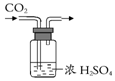 干燥二氧化碳 | B. | 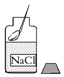 取少量氯化钠 | C. |  二氧化碳验满 | D. |  加热液体 |
 (1)为了预防佝偻病,幼儿及青少年每日必须摄入足够量的钙元素;
(1)为了预防佝偻病,幼儿及青少年每日必须摄入足够量的钙元素;
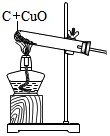 将炭粉和氧化铜的混合物共15g装入试管中(如图装置),加热一段时间后(发生反应2CuO+C═2Cu+CO2↑)冷却、称量,发现剩余固体质量为12.8g.求
将炭粉和氧化铜的混合物共15g装入试管中(如图装置),加热一段时间后(发生反应2CuO+C═2Cu+CO2↑)冷却、称量,发现剩余固体质量为12.8g.求