题目内容
(2005?常德)某化学活动兴趣小组的同学进行木炭还原氧化铜的探究实验,生成物是红色固体和无色气体.他们通过查阅资料后,得知氧化亚铜(Cu2O)为红色固体,因此,猜测生成物里有CO和Cu,还可能有CO和Cu2O.又知Cu2O能和常见的酸(HNO3除外)反应生成Cu2+和Cu.为此,请你和他们一起进行如下探究.(1)探究气体中是否有CO气体:甲同学设计的方案是:将气体干燥后,再通过灼热的氧化铜,未反应完的气体直接排放到空气中.乙同学设计的方案是:将气体通过足量的氢氧化钠溶液后,干燥,再点燃.
①甲同学实验后如果有______色固体生成,说明一定含有CO气体;
②上述两种方案中可选用的一种气体干燥剂是______;
③从空气污染的角度考虑,你认为上述两种方案中______同学的方案更好,你的理由是______.
(2)探究红色固体中是否有Cu2O:
①在如下方法中:a.上网查询 b.实验 c.请教老师
猜想你认为最能解决实际问题的方法是______(填字母序号).
②请你设计一个简便的实验方案,检验红色固体中是否有Cu2O.
| 实 验 步 骤 | |
| 实验现象与结论 | |
| 化学反应方程式 |
【答案】分析:(1)①叙述现象主要从物理性质方面分析反应物和生成物;②CO的化学性质比较稳定,只有在高温下才反应,所以干燥剂比较多③评价实验方案的合理性主要从方案是否完成实验目的、是否简便易操作、是否安全等角度分析.
(2)①化学是一门以实验为基础的学科,实验是最好的老师.②关键要分析实验目的,结合信息进行设计.
解答:解:(1)①反应的化学方程式为CO+CuO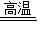 Cu+CO2有红色的铜生成.
Cu+CO2有红色的铜生成.
②CO性质比较稳定,常温下一般不参与反应,所以干燥剂很多,如浓硫酸、固体氢氧化钠、碱石灰、固体氯化钙等.
③从反应的操作性分析乙同学反应条件低,简便;从实验安全性分析甲同学没有对尾气CO处理.所以乙同学方案比较好
(2)①化学是一门以实验为基础的学科,实验是最好的老师,选b.
②实验目的是检验红色固体中含有Cu2O,根据题意Cu2O和硫酸反应生成Cu和Cu 2+,而Cu不和稀硫酸反应,所以可用硫酸铜的颜色来区别.若溶液变为蓝色证明有Cu2O存在.
故答案为:
(1)①红②浓硫酸(或固体氢氧化钠、碱石灰、固体氯化钙)
③乙,因为甲同学的方案没有对尾气进行处理
(2)①b ②
点评:本题从化学方程式的书写、实验方案的评价、实验设计多角度考查了学生实验能力.
(2)①化学是一门以实验为基础的学科,实验是最好的老师.②关键要分析实验目的,结合信息进行设计.
解答:解:(1)①反应的化学方程式为CO+CuO
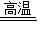 Cu+CO2有红色的铜生成.
Cu+CO2有红色的铜生成.②CO性质比较稳定,常温下一般不参与反应,所以干燥剂很多,如浓硫酸、固体氢氧化钠、碱石灰、固体氯化钙等.
③从反应的操作性分析乙同学反应条件低,简便;从实验安全性分析甲同学没有对尾气CO处理.所以乙同学方案比较好
(2)①化学是一门以实验为基础的学科,实验是最好的老师,选b.
②实验目的是检验红色固体中含有Cu2O,根据题意Cu2O和硫酸反应生成Cu和Cu 2+,而Cu不和稀硫酸反应,所以可用硫酸铜的颜色来区别.若溶液变为蓝色证明有Cu2O存在.
故答案为:
(1)①红②浓硫酸(或固体氢氧化钠、碱石灰、固体氯化钙)
③乙,因为甲同学的方案没有对尾气进行处理
(2)①b ②
| 实验步骤 | 取少量红色固体于试管中,滴加稀硫酸,振荡 |
| 实验现象与结论 | 如果溶液变蓝,一定含有Cu2O |
| 化学反应方程式 | Cu2O+H2SO4=Cu+H2O+CuSO4 |
点评:本题从化学方程式的书写、实验方案的评价、实验设计多角度考查了学生实验能力.

练习册系列答案
相关题目
(2005?常德)某同学去我市石门县壶瓶山风景区游玩,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,他称取10.0g样品,将60.0g稀盐酸分四次加入,测量的有关数据见下表(已知样品中的杂质不溶于水,且不与稀酸盐反应).
求:(1)样品中碳酸钙的质量分数;
(2)10.0g该样品与足量稀盐酸反应后可产生二氧化碳多少克?(计算结果精确到小数点后两位)
| 加入稀盐酸的次序 | 1 | 2 | 3 | 4 |
| 加入稀盐酸的质量(g) | 15.0 | 15.O | 15.0 | 15.0 |
| 剩余固体的质量(g) | 7.O | 4.O | 1.O | 1.O |
(2)10.0g该样品与足量稀盐酸反应后可产生二氧化碳多少克?(计算结果精确到小数点后两位)
(2005?常德)某同学去我市石门县壶瓶山风景区游玩,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,他称取10.0g样品,将60.0g稀盐酸分四次加入,测量的有关数据见下表(已知样品中的杂质不溶于水,且不与稀酸盐反应).
求:(1)样品中碳酸钙的质量分数;
(2)10.0g该样品与足量稀盐酸反应后可产生二氧化碳多少克?(计算结果精确到小数点后两位)
| 加入稀盐酸的次序 | 1 | 2 | 3 | 4 |
| 加入稀盐酸的质量(g) | 15.0 | 15.O | 15.0 | 15.0 |
| 剩余固体的质量(g) | 7.O | 4.O | 1.O | 1.O |
(2)10.0g该样品与足量稀盐酸反应后可产生二氧化碳多少克?(计算结果精确到小数点后两位)
 (2006?常德)2005年11月13日,吉林石化公司双苯厂某车间因意外发生连续爆炸,对附近的松花江造成了污染.
(2006?常德)2005年11月13日,吉林石化公司双苯厂某车间因意外发生连续爆炸,对附近的松花江造成了污染.