题目内容
13.下列是初中化学中三个实验,请按要求填空: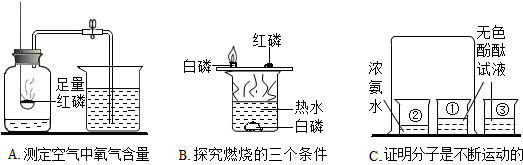
(1)C实验中产生的现象是①中酚酞变红烧杯③的作用是与①进行对比试验.
(2)A实验中红磷燃烧的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,实验说明氧气的体积约占空气的$\frac{1}{5}$,该实验成功的关键是①②③④(填序号)
①装置气密性好②实验前夹紧止水夹③红磷过量或足量④冷却到室温后才打开止水夹⑤要选用教室中的空气
(3)B实验中,由钢片上的白磷燃烧而热水中的白磷没有燃烧的现象可以得知:可燃物燃烧的条件之一是:可燃物要与氧气接触.
(4)实验时,不慎将将酒精洒到桌面并着火,可用湿布覆盖,其灭火原理是隔绝空气.
分析 (1)通过烧杯①与烧杯③的对比发现,烧杯①中的酚酞变红,烧杯③中的酚酞不变色,说明是氨水让酚酞变红而不是其它物质让酚酞变红,而氨水和酚酞并没有混合,从而说明分子是在不断的运动.
(2)根据空气中氧气的体积分数分析;根据实验的过程及注意的事项分析;
(3)考虑可燃物燃烧的条件;
(4)根据灭火的原理来分析.
解答 解:(1)通过烧杯①与烧杯③的对比发现,烧杯①中的酚酞变红,烧杯③中的酚酞不变色,说明是氨水让酚酞变红而不是其它物质让酚酞变红,而氨水和酚酞并没有混合,从而说明分子是在不断的运动.故答案为:①中酚酞变红;与①进行对比试验.
(2)红磷燃烧的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.由于空气中氧气的体积分数约占空气体积的$\frac{1}{5}$.所以,C实验说明氧气的体积约占空气的$\frac{1}{5}$;实验成功的关键与许多因素有关,如果装置漏气、实验前未夹紧止水夹,红磷的量不足,未冷却后再打开止水夹都是使测得结果偏小.故填:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;$\frac{1}{5}$;①②③④;
(3)B实验中,由铜片上白磷燃烧而热水中的白磷没有燃烧的现象可以得知,可燃物燃烧的条件之一是:可燃物与氧气接触才能燃烧.故答案为:可燃物要与氧气接触;
(4)实验时,不慎将酒精洒到桌面并着火,可用湿布覆盖,其灭火原理是:隔绝空气.故填:隔绝空气.
点评 此题以图示的形式综合考查了正确判断实验现象及规范进行基本的实验操作的综合题.解题时应充分利用题中给予的信息,进行筛选分析,得出正确答案.

练习册系列答案
相关题目
4.某同学向过氧化氢溶液中加入二氧化锰制取氧气,相关数据如表:
请计算:
(1)过氧化氢中,氢元素与氧元素的质量之比为1:16.
(1)该同学制得氧气的质量为1.6g.
(2)该同学所用过氧化氢溶液的溶质质量分数.
| 反应前物质的质量/g | 充分反应后物质的质量/g | |
| 过氧化氢溶液 | 二氧化锰 | 固体与液体混合物质量 |
| 68.0 | 0.1 | 66.5 |
(1)过氧化氢中,氢元素与氧元素的质量之比为1:16.
(1)该同学制得氧气的质量为1.6g.
(2)该同学所用过氧化氢溶液的溶质质量分数.
18.下列做法不能防止金属锈蚀的是( )
| A. | 与其他金属仪器制成合金 | B. | 在金属制品表面涂油漆 | ||
| C. | 在金属制品表面上一层釉 | D. | 保留铁盆上的铁锈 |
5.现有40g溶质质量分数为5%的氯化钠溶液,若使该溶液的溶质质量分数变为20%,则需要蒸发掉的水(恒温蒸发)的质量为( )
| A. | 15g | B. | 20g | C. | 25g | D. | 30g |
2.下列有关碳及其化合物的说法正确的是( )
| A. | 二氧化碳是引发酸雨的“罪魁祸首” | |
| B. | 大气中消耗二氧化碳的主要途径是绿色植物的呼吸作用 | |
| C. | 室内放一盆水能防止一氧化碳中毒 | |
| D. | 金刚石和石墨物理性质不同是因为它们的碳原子排列顺序不同 |