题目内容
12.一定条件下,下表所示的物质在密闭的容器内充分反应,测得反应前后各物质的质量如下表:| 物质 | X | 氧气 | 水 | 二氧化碳 | 一氧化碳 |
| 反应前质量/g | 3.2 | 11.2 | 0 | 0 | 0 |
| 反应前质量/g | 0 | 0 | 7.2 | 4.4 | a |
分析 根据质量守恒定律,计算生成一氧化碳的质量为:3.2g+11.2g-7.2g-4.4g=2.8g,然后依据相同条件下,气体的体积比即分子个数比进行计算.
解答 解:依据质量守恒定律,生成一氧化碳的质量为:3.2g+11.2g-7.2g-4.4g=2.8g,相同条件下,气体的体积比即分子个数比:$\frac{2.8g}{28}$:$\frac{4.4g}{44}$=1:1,
需增加的氧气的质量为x
2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2,
56 32
2.8g x
$\frac{56}{2.8g}$=$\frac{32}{x}$
x=1.6g
所以需增加的氧气的质量为1.6g.
故答案为:1:1,1.6g
点评 本题主要考查了质量守恒定律的应用,难度不大,需要在平时多加训练.

练习册系列答案
相关题目
20.菠萝味的饮料中通常加的是丁酸乙酯,化学式为C6H12O2,下列说法正确的是( )
| A. | 丁酸乙酯由20个原子构成 | |
| B. | 一个丁酸乙酯分子中碳、氢、氧原子的个数比为3:6:2 | |
| C. | 丁酸乙酯中氢元素的质量分数最小 | |
| D. | 丁酸乙酯的相对分子质量是116g |
17.下列说法中不正确的是( )
| A. | 甲烷是最简单的有机物 | |
| B. | 氮、磷、钾是农作物所需的三种基本元素 | |
| C. | 铜用来制造炮弹是因为铜具有导电性 | |
| D. | 浓硫酸可以作为干燥剂是因为它具有吸水性 |
1.下列各物质中,能用金属与盐酸反应直接制取的是( )
| A. | CuCl2 | B. | FeCl3 | C. | AlCl3 | D. | AgCl |

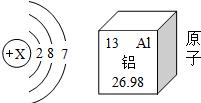 某元素A的原子结构示意图如图所示,图中X=17,该元素的原子在化学反应中易得到(填“得到”或“失去”)电子形成离子,该离子的符号是Cl-,它与钠元素形成化合物的化学式NaCl.铝元素的相对原子质量是26.98.
某元素A的原子结构示意图如图所示,图中X=17,该元素的原子在化学反应中易得到(填“得到”或“失去”)电子形成离子,该离子的符号是Cl-,它与钠元素形成化合物的化学式NaCl.铝元素的相对原子质量是26.98.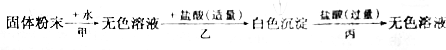
 ,由此可写出各步反应的化学方程式.
,由此可写出各步反应的化学方程式. .
.