题目内容
7.氮是一种地球上含量丰富的元素.如图表示氮及其化合物在一定条件下的转化关系: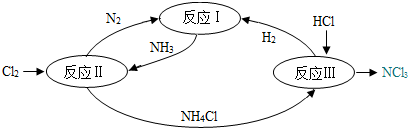
(1)氮元素在不同的物质中存在循环,体现了化学反应前后元素种类不变.
(2)反应II中,发生化学反应的基本反应类型是置换反应.
(3)反应III中,发生反应的化学方程式为NH4Cl+2HCl═NCl3+3H2.
分析 (1)化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变;
(2)根据反应物、生成物的种类可以判断反应类型;
(3)根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式.
解答 解:(1)氮元素在不同的物质中存在循环,体现了化学反应前后元素种类不变.
故填:元素种类.
(2)反应II中,发生反应的化学方程式为:8NH3+3Cl2=6NH4Cl+N2,属于置换反应.
故填:置换反应.
(3)反应III中,NH4Cl和HCl反应生成了NCl3和H2,发生反应的化学方程式为:NH4Cl+2HCl═NCl3+3H2.
故填:NH4Cl+2HCl═NCl3+3H2.
点评 化学反应前后,元素种类不变,原子种类也不变,因此(1)也可以填原子种类或元素和原子种类,要注意理解.

练习册系列答案
相关题目
10.除去下列物质中的少量杂质,所选用的试剂及操作方法 均正确的是( )
| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | CO2气体(CO) | 过量的氧气 | 点燃 |
| B | Fe2O3(Fe) | 足量的盐酸 | 过滤 |
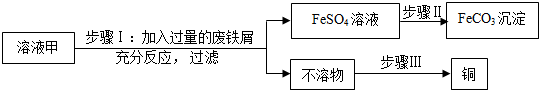
| C | FeSO4溶液(CuSO4) | 足量的锌 | 过滤 |
| D | O2(H2O) | 浓硫酸 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
19.将海水淡化与浓海水资源化结合起来是综合利用海水的重要途径之一.一般是先将海水淡化,再从剩余的浓海水中通过一系列工艺流程提取其他产品.
(1)海水提取镁的一段工艺流程如图:
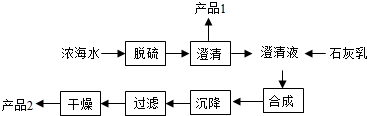
浓海水的主要成分如表:
该工艺流程中需要对海水进行脱硫,原理是用钙离子沉淀硫酸根离子,产品1为CaSO4,过滤后干燥的产品2为氢氧化镁,该反应方程式为MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2;1L浓海水最多可得到产品2的质量为69.6g.
(2)采用石墨阳极、不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑;电解时,若有少量水存在会造成产品镁与水在高温下反应生成碱与氢气,该反应的化学方程式Mg+2H2O$\frac{\underline{\;高温\;}}{\;}$Mg(OH)2+H2↑.
(3)如图所示:海水经过晒盐后得到粗盐和苦卤,粗盐中还含有Ca2+、Mg2+、SO42-等可溶性杂质,以下是某化工厂进行粗盐提纯的示意图:
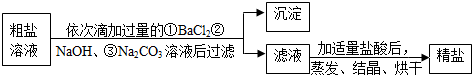
过量试剂①②③的顺序也可调整为②①③,过滤后可得到四种沉淀的化学式为Mg(OH)2、BaSO4、CaCO3、BaCO3;在利用粗盐制备精盐过程中,加入适量盐酸的目的是除去溶液中含有的NaOH,Na2CO3(填物质的化学式).
(4)利用井盐和合成氨生产的氨气及二氧化碳生产纯碱的“联合制碱法”是由我国著名化学家侯德傍先生发明的,其氯化钠的利用率高达96%.其原理流程如图所示:
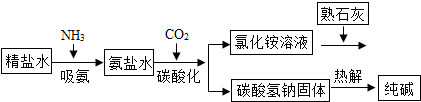
①氨极易溶于水,向饱和食盐水通入氨气可得到饱和食盐水和氨水的混合盐水(称为氨盐水),氨盐水比食盐水更容易吸收二氧化碳,其原因是氨盐水显碱性;
②写出氯化铵溶液与熟石灰反应的化学方程式2NH4Cl+Ca(OH)2═CaCl2+2H2O+2NH3↑.
(1)海水提取镁的一段工艺流程如图:

浓海水的主要成分如表:
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/(g•L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
(2)采用石墨阳极、不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑;电解时,若有少量水存在会造成产品镁与水在高温下反应生成碱与氢气,该反应的化学方程式Mg+2H2O$\frac{\underline{\;高温\;}}{\;}$Mg(OH)2+H2↑.
(3)如图所示:海水经过晒盐后得到粗盐和苦卤,粗盐中还含有Ca2+、Mg2+、SO42-等可溶性杂质,以下是某化工厂进行粗盐提纯的示意图:

过量试剂①②③的顺序也可调整为②①③,过滤后可得到四种沉淀的化学式为Mg(OH)2、BaSO4、CaCO3、BaCO3;在利用粗盐制备精盐过程中,加入适量盐酸的目的是除去溶液中含有的NaOH,Na2CO3(填物质的化学式).
(4)利用井盐和合成氨生产的氨气及二氧化碳生产纯碱的“联合制碱法”是由我国著名化学家侯德傍先生发明的,其氯化钠的利用率高达96%.其原理流程如图所示:

①氨极易溶于水,向饱和食盐水通入氨气可得到饱和食盐水和氨水的混合盐水(称为氨盐水),氨盐水比食盐水更容易吸收二氧化碳,其原因是氨盐水显碱性;
②写出氯化铵溶液与熟石灰反应的化学方程式2NH4Cl+Ca(OH)2═CaCl2+2H2O+2NH3↑.
16.如图是某同学用于测定空气中氧气含量的装置.下列说法错误的是( )
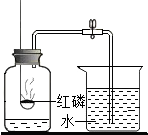

| A. | 实验前一定要检查装置的气密性 | |
| B. | 该实验得出的结论是氧气占空气总体积的$\frac{1}{5}$ | |
| C. | 燃烧的红磷熄灭后,立刻打开止水夹 | |
| D. | 实验时红磷一定要过量,并预先在集气瓶底放少量的水 |
17.只用水作试剂,不可能区分开来的一组物质是( )
| A. | 食盐、碳酸钠 | B. | 酒精、浓硫酸 | C. | 碳酸钙、碳酸钠 | D. | 硫酸铜、硝酸钠 |