题目内容
15.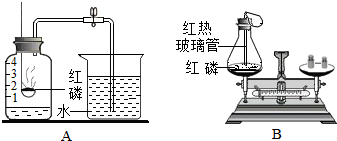 根据如图实验装置回答问题:
根据如图实验装置回答问题:(1)A图的实验目的是测定空气中氧气含量;若装置的气密性不好,导致的后果是什么?
(2)B图是探究质量守恒定律的实验,请从微观角度解释质量守恒定律.
(3)写出上述实验中发生的化学反应方程式.
分析 (1)实验A可以测出空气中氧气的含量,待集气瓶中的红磷熄灭,冷却后打开弹簧夹,烧杯中的水进入集气瓶中,液面约上升到刻度1处;
(2)根据质量守恒定律的微观实质回答;
(3)根据磷和氧气在点燃的条件下反应生成五氧化二磷解答.
解答 解:(1)实验A可以测出空气中氧气的含量,即氧气约占空气总量的$\frac{1}{5}$;若装置的气密性不好,导致的后果是氧气的体积分数小于空气总量的$\frac{1}{5}$;
(2)从微观角度分析化学反应遵守质量守恒定律的原因是原子的“三个不变”,即化学反应前后原子的种类、数目、质量都没有发生改变;
(3)磷和氧气在点燃的条件下反应生成五氧化二磷;发生的化学反应方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
答案:
(1)测定空气中氧气含量;氧气的体积分数小于空气总量的$\frac{1}{5}$;
(2)化学反应前后原子的种类、数目、质量都没有发生改变;
(3)4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
点评 本题考查了对空气中氧气的测定以及质量守恒定律,让学生通过实验探究去理解、掌握这些知识.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
5.空气中体积分数最小的气体是( )
| A. | 氮气 | B. | 氧气 | C. | 二氧化碳 | D. | 稀有气体 |
6.下列除去杂质的方法中,不正确的是( )
| A. | NaOH溶液(Na2CO3),加入适量的Ca(OH)2溶液、过滤 | |
| B. | CaO(CaCO3),加水溶解、过滤 | |
| C. | CO(CO2),通过足量的NaOH溶液、干燥 | |
| D. | FeSO4溶液(H2SO4),加入足量Fe粉、过滤 |
3.物质的性质决定用途,下列物质的用途由其化学性质决定的是( )
| A. | 用钢丝做导线 | B. | 用活性炭除去冰箱的异味 | ||
| C. | 用氦气填充食品袋内以防腐 | D. | 用金刚石做钻探机的钻头 |
20.下列反应能发生且化学方程式正确的是( )
| A. | CaCO3+Cu(OH)2═Ca(OH)2+CuCO3↓ | B. | Cu+H2SO4═CuSO4+H2↑ | ||
| C. | Fe(OH)3+3HCl═FeCl3+3H2O | D. | NaOH+KNO3═KOH+NaNO3 |
7.下列物质的名称、化学式和所属的类别都正确的是( )
| A. | 甲烷、CH4、混合物 | B. | 锰、Mn、金属单质 | ||
| C. | 氯酸钾、KClO3、金属氧化物 | D. | 氧化汞、HgO、非金属氧化物 |
4.向紫色石蕊中通入CO2气体,等溶液变色后,将它放在酒精灯上加热,直到溶液颜色不再发生变化为止,本实验过程中观察到的溶液颜色变化是( )
| A. | 紫色→红色→白色 | B. | 紫色→红色→紫色 | C. | 紫色→紫色→红色 | D. | 紫色→红色→无色 |