题目内容
2.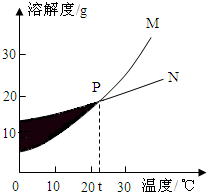 如图表示M、N两种固体物质的溶解度曲线,下列说法正确的是( )
如图表示M、N两种固体物质的溶解度曲线,下列说法正确的是( )| A. | 除去M中混有的少量N应用蒸发结晶 | B. | M、N都不是易溶物质 | ||
| C. | P点表示t℃时M、N的溶解度相等 | D. | 阴影处M、N均为饱和溶液 |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:A、M物质的溶解度受温度的影响较大,所以除去M中混有的少量N应用降温结晶,故A错误;
B、M、N两种物质在20℃时的溶解度是20,所以M、N都是易溶物质,故B错误;
C、P点表示t℃时,M、N的溶解度相等,故C正确;
D、通过分析溶解度曲线可知,阴影处M为饱和溶液,N是不饱和溶液,故D错误.
故选:C.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
12.以下四组物质的溶液,不另加试剂就可将它们区分开的是( )
| A. | HCl Na2CO3 HNO3 NaCl | B. | Na2CO3 Na2SO4 BaCl2 NaCl | ||
| C. | NaCl NaOH FeCl3 KNO3 | D. | CuSO4 MgCl2 NaOH Na2SO4 |
17.溶液在日常生活及工农业生产上具有广泛的用途.
(1)医疗上常用0.9%NaCl溶液作生理盐水,生理盐水中的溶质是氯化钠.
(2)已知KCl的溶解度20°C时为34g,40°C时为40g.某实验小组做了如图实验.

①C所得溶液中溶质与溶剂的质量比为2:5;
②A~E所得溶液中,没有固体剩余的溶液是AD(填序号,下同),溶质的质量分数相等的是B与E和C与D.溶质的质量分数最大的是C、D.
(1)医疗上常用0.9%NaCl溶液作生理盐水,生理盐水中的溶质是氯化钠.
(2)已知KCl的溶解度20°C时为34g,40°C时为40g.某实验小组做了如图实验.

| 温度 | 溶解度 | 溶质质量 | 溶剂质量 | 是否饱和 | 有无晶体 | 溶质质量分数 | |
| A | |||||||
| B | |||||||
| C | |||||||
| D | |||||||
| E |
②A~E所得溶液中,没有固体剩余的溶液是AD(填序号,下同),溶质的质量分数相等的是B与E和C与D.溶质的质量分数最大的是C、D.
14.下列有关质量守恒定律的认识,正确的是( )
| A. | 质量守恒定律揭示了化学变化中宏观物质之间的质量关系,与微观过程无关 | |
| B. | 3g碳和10g氧气充分反应后,得到二氧化碳的质量为13g | |
| C. | 质量守恒定律为定量揭示化学变化的规律,提供了理论依据 | |
| D. | 煤块充分燃烧后,煤灰的质量小于煤块的质量,该反应不遵循质量守恒定律 |
11.物质的性质决定了物质的用途.下列几种常见物质的性质、用途不一致的是( )
| A. | 氮气 性质稳定 保护气 | |
| B. | 酒精 可燃性 消毒剂 | |
| C. | 食醋 酸性 除水垢 | |
| D. | 干冰 升华吸热 人工降雨 |
12.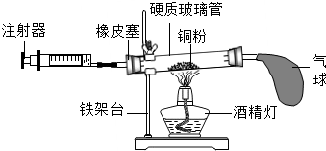 用如图所示装置来测定空气中氧气的含量,对该实验认识错误的是( )
用如图所示装置来测定空气中氧气的含量,对该实验认识错误的是( )
 用如图所示装置来测定空气中氧气的含量,对该实验认识错误的是( )
用如图所示装置来测定空气中氧气的含量,对该实验认识错误的是( )| A. | 气球的作用主要是调节气压,使氧气完全反应 | |
| B. | 实验结束后冷却到室温才能读数 | |
| C. | 反应结束后消耗氧气的总体积应该是反应前容器内气体总体积的$\frac{1}{5}$ | |
| D. | 铜粉用量的多少,不会影响实验结果 |
 已知某金属X有下列相关信息:①它的主要矿物的化学成分是X2O3;②它主要通过热还原法冶炼而成;③它的年产量位于金属之首.
已知某金属X有下列相关信息:①它的主要矿物的化学成分是X2O3;②它主要通过热还原法冶炼而成;③它的年产量位于金属之首.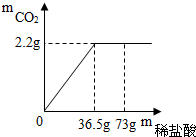 现有7.5g石灰石样品于稀盐酸反应制取二氧化碳气体,反应产生的二氧化碳气体的质量与加入的稀盐酸的质量关系如图所示.(友情提示:石灰石样品中的杂质不溶于水,也不发生反应)
现有7.5g石灰石样品于稀盐酸反应制取二氧化碳气体,反应产生的二氧化碳气体的质量与加入的稀盐酸的质量关系如图所示.(友情提示:石灰石样品中的杂质不溶于水,也不发生反应)