题目内容
7.下列记录的实验现象与事实不相符的是( )| A. | 磷在空气中燃烧产生大量白烟 | |
| B. | 打开盛有浓盐酸的试剂瓶,看到瓶口有大量白雾 | |
| C. | 取少量氢氧化钠曝露在空气中,氢氧化钠表面潮湿并逐渐溶解 | |
| D. | 在电解水的实验中,正负两极产生的气体体积比约为2:1 |
分析 A、根据磷在空气中燃烧的现象进行分析判断.
B、根据浓盐酸具有挥发性进行分析判断.
C、根据氢氧化钠易潮解进行分析判断.
D、根据电解水的实验现象进行分析判断.
解答 解:
A、磷在空气中燃烧,产生大量的白烟,故选项说法正确.
B、浓盐酸具有挥发性,打开盛有浓盐酸的试剂瓶,看到瓶口有大量白雾,故选项说法正确.
C、氢氧化钠易潮解,取少量氢氧化钠露在空气中,氢氧化钠表面潮湿并逐渐溶解,故选项说法正确.
D、在电解水实验中,可观察到:与电源正极相连的试管内产生的气体体积少,与电源负极相连的试管内的气体体积多;且两者的体积之比大约是1:2,故选项说法错误.
故选:D.
点评 本题难度不大,掌握常见物质燃烧的现象、浓盐酸具有挥发性、电解水的实验现象、氢氧化钠易潮解即可正确解答,在描述实验现象时,需要注意烟和雾的区别.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.初中化学要求学生必须掌握规范的实验操作,下列实验操作符合规范要求的是( )
| A. |  熄灭酒精灯 | B. | 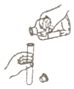 倾倒液体 | C. | 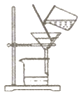 过滤泥浆水 | D. |  滴加液体 |
18.下列各组常见的固体物质中,用水不能区分的是( )
| A. | NaOH和NH4NO3 | B. | Fe2(SO4)3 和Na2SO4 | ||
| C. | Na2CO3和CaCO3 | D. | CaCl2和KCl |
15.逻辑推理是一种重要的化学思维方法.以下推理正确的是( )
| A. | 酸碱中和反应有水生成,有水生成的反应一定是酸碱中和反应 | |
| B. | NaCl溶液能够导电,则所有溶液都能导电 | |
| C. | 化学变化中分子种类发生改变,分子种类发生改变的变化一定是化学变化 | |
| D. | 酸溶液能使紫色石蕊试液变红,能使紫色石蕊试液变红的一定是酸溶液 |
2.实验是学习化学的灵魂,下列基本实验操作中正确的是( )
| A. | 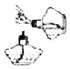 点燃酒精灯 | B. |  配置溶液 | C. | 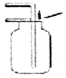 二氧化碳验满 | D. |  倾倒液体 |
16.古诗词中也能体现化学之美,下列诗句不涉及化学变化的是( )
| A. | 野火烧不尽,春风吹又生 | B. | 蚕到死丝方尽,蜡炬成灰泪始干 | ||
| C. | 千里冰封,万里雪飘 | D. | 千锤万凿出深山,烈火焚烧若等闲 |
17.已知某金属粉末中除含有Al外还含有一定量的Fe,为测定金属的含量,某化学兴趣小组的同学展开了如下的实验探究.
小资料:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH═2NaAlO2+3H2↑,Fe不与氢氧化钠溶液反应).取20g该金属粉末,把100g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据如下:
试分析回答下列问题:
(1)上表中m的值为9.9;
(2)Fe的质量分数为49.5%;
(3)第五次加入NaOH后,溶液中的溶质是氢氧化钠和偏铝酸钠;
(4)列式计算:所用氢氧化钠溶液的溶质质量分数为多少?
小资料:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH═2NaAlO2+3H2↑,Fe不与氢氧化钠溶液反应).取20g该金属粉末,把100g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据如下:
| 加NaOH溶液的次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 剩余固体的质量/g | 17.3 | 14.6 | 11.9 | 9.9 | m |
(1)上表中m的值为9.9;
(2)Fe的质量分数为49.5%;
(3)第五次加入NaOH后,溶液中的溶质是氢氧化钠和偏铝酸钠;
(4)列式计算:所用氢氧化钠溶液的溶质质量分数为多少?
