题目内容
4.现有如图A、B、C、D、E五种实验装置: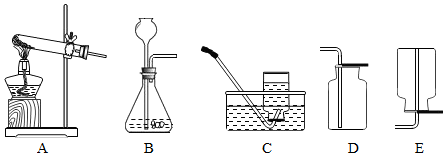
根据题意,将装置的序号填入下列空格中.
(1)写出你喜欢的两种仪器的名称酒精灯,试管.
(2)加热高锰酸钾制取氧气,用A装置,收集氧气最好用CD装置.写出加热高锰酸钾制取氧气的文字表达式高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.
(3)用过氧化氢溶液与二氧化锰制取氧气,用B装置.写出用过氧化氢溶液与二氧化锰制取氧气的文字表达式过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
(4)氨气极易溶于水,且密度比空气小,实验室常用加热固体硫酸铵和固体熟石灰的混合物来制取氨气,应用A装置,收集氨气最好用E装置.
分析 (1)根据实验室常用仪器解答;
(2)根据如果用高锰酸钾就需要加热,根据氧气不易溶于水,密度比空气的密度大解答;
(3)根据如果用过氧化氢和二氧化锰制氧气,就不需要加热.要注意文字表达式的书写.
(4)依据药品的状态和反应条件来选择发生装置,依据气体的密度与水溶性来选择气体的收集装置.
解答 解:(1)试管和酒精灯是实验室常用的两种仪器,故答案为:试管;酒精灯;
(2)如果用高锰酸钾就需要加热,氧气不易溶于水,密度比空气的密度大,因此可以用排水法和向上排空气法收集,其中排水法收集的气体比较纯净.
加热高锰酸钾制取氧气的文字表达式为:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;
(3)用过氧化氢和二氧化锰制氧气,就不需要加热.因此发生装置为B,文字表达式为:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
(4)用加热固体硫酸铵和固体熟石灰的混合物来制取氨气,所以我们选择A装置来制气体.又因氨气极易溶于水,且密度比空气小,所以我们只能用向下排空气法来收集氨气.
故答案为:
(1)酒精灯;试管;
(2)A;C;高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;
(3)B;过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;
(4)A;E.
点评 本考点主要考查气体的制取装置和收集装置的选择,同时也考查了文字表达式的书写,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
15.对于图示 理解错误的是( )
理解错误的是( )
 理解错误的是( )
理解错误的是( )| A. | 原子可结合分子 | |
| B. | 可用 表示分子的形成过程 表示分子的形成过程 | |
| C. | 化学变化的基础是分子的破裂和原子的重新组合 | |
| D. | 物质都是由分子构成 |
12.向含有AgNO3、Cu (NO3)2、Zn (NO3)2的混合溶液中加人一定量的铁粉,使其充分反应后,过滤,向滤渣中滴加稀盐酸,有气泡产生,则下列结论不正确的是( )
| A. | 滤渣中只含有Fe | |
| B. | 滤渣中一定含有Ag、Cu、Zn | |
| C. | 滤渣中一定含有Ag、Cu、Fe | |
| D. | 滤液中一定含Zn2+、不含Fe2+、Cu2+、Ag+ |
16.小亮在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度.于是他对所得溶液的酸碱性进行探究.
【探究目的】探究所得溶液的酸碱性
【提出猜想】所得溶液可能呈碱性,也可能呈中性,还可能呈酸性.
【实验验证】
【分析与思考】
(1)若溶液呈碱性,则溶液中使其呈碱性的离子是OH-(填写微粒符号),为避免碱性溶液污染环境,小亮对所得溶液进行了如下处理:向溶液中逐滴加入一种FeCl3溶液,直到不再产生沉淀为止.然后过滤,把滤液倒入蒸发皿中加热,得到氯化钠晶体.
(2)若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:
方案一:取样,加入碳酸钠溶液,若观察到有气泡产生,则所取溶液呈性;若无明显现象,则呈中性.
方案二:取样,加入金属锌,若有有气泡产生产生,则所取溶液呈酸性,该反应的化学方程式为Zn+2HCl=ZnCl2+H2↑;若无明显现象,则呈中性.
【探究目的】探究所得溶液的酸碱性
【提出猜想】所得溶液可能呈碱性,也可能呈中性,还可能呈酸性.
【实验验证】
| 实验操作 | 实验现象 | 结论 |
| 用试管取该溶液1-2mL,滴入1-2滴无色酚酞试液,振荡 | 无色酚酞试液变红 | 溶液呈碱性 |
| 无色酚酞试液不变色 | 溶液呈中性或酸性 |
(1)若溶液呈碱性,则溶液中使其呈碱性的离子是OH-(填写微粒符号),为避免碱性溶液污染环境,小亮对所得溶液进行了如下处理:向溶液中逐滴加入一种FeCl3溶液,直到不再产生沉淀为止.然后过滤,把滤液倒入蒸发皿中加热,得到氯化钠晶体.
(2)若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:
方案一:取样,加入碳酸钠溶液,若观察到有气泡产生,则所取溶液呈性;若无明显现象,则呈中性.
方案二:取样,加入金属锌,若有有气泡产生产生,则所取溶液呈酸性,该反应的化学方程式为Zn+2HCl=ZnCl2+H2↑;若无明显现象,则呈中性.
13.百合有润肺止咳功效,百合中含秋水仙碱,化学式为C22H25NO6,下列说法正确的是( )
| A. | 秋水仙碱由碳、氢、氧三种元素组成 | |
| B. | 秋水仙碱中氢元素的质量分数最大 | |
| C. | 一个秋水仙碱分子由22个碳原子、25个氢原子、1个氮原子和3个氧分子构成 | |
| D. | 秋水仙碱分子中碳、氢、氮、氧原子个数比为22:25:1:6 |
4.小明是一名“小马虎”,他在用高锰酸钾制取氧气,并进行氧气性质实验时遇到了下列问题,请你帮他解决.

(1)水槽中的水变成了红色,原因是没有在试管口放一团棉花.
(2)做细铁丝在氧气中燃烧的实验时,没有看到“剧烈燃烧,火星四射”的现象,你认为实验失败的可能原因:(至少写两条):①氧气不纯;②铁丝表面的铁锈没有清理干净等.
(3)小红对小明的实验进行了改进,并对铁丝在氧气中燃烧时“火星四射”的现象与其含碳量的关系进行了如下探究.

(1)水槽中的水变成了红色,原因是没有在试管口放一团棉花.
(2)做细铁丝在氧气中燃烧的实验时,没有看到“剧烈燃烧,火星四射”的现象,你认为实验失败的可能原因:(至少写两条):①氧气不纯;②铁丝表面的铁锈没有清理干净等.
(3)小红对小明的实验进行了改进,并对铁丝在氧气中燃烧时“火星四射”的现象与其含碳量的关系进行了如下探究.
| 实验操作 | 实验现象 | 解释与结论 |
| 实验①:取直径0.20mm,含碳0.1%的铁丝,在氧气中燃烧 | 零星的火星 | ①分别用物质名称和化学符号写出铁燃烧的化学反应表达式:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4; ②铁丝在氧气中燃烧,“火星四射”与其含碳量的关系为含碳量越高,产生的火星越多 |
| 实验②:取直径0.20mm,含碳0.32%的铁丝,在氧气中燃烧 | 较明显的火星四射 |