题目内容
2.化学成为一门科学开始于( )| A. | 对燃烧现象的深入研究 | |
| B. | 对空气组成的研究 | |
| C. | 铁的冶炼和使用 | |
| D. | 用原子-分子论来研究化学反应之后 |
分析 分析化学的发展史,理清各种成就的先后顺序,然后得出明确结果.
解答 解:A、对燃烧现象的深入研究,研究出燃烧的本质的科学家是拉瓦锡,是在化学成为一门学科之后,故A错误.
B、对空气组成的研究典型实验也是拉瓦锡做的,是在化学成为一门学科之后,故B错误.
C、铁的冶炼和利用,是在化学成为一门学科之后,故C错误.
D、自从原子-分子论的确立,奠定了近代化学的基础,此后化学才成为一门真正的学科,故D正确.
故选:D.
点评 了解化学发展史,是对前人成就的恳定,也是我们为化学发展而奋斗的动力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.加热条件下,将24g CuO、Fe2O3的混合物与充足的CO完全反应,并将反应后的气体全部通入到澄清石灰水中,得到白色沉淀40g.下列有关叙述中不正确的是( )
| A. | 原混合物中CuO与Fe2O3物质的量的比为1:1 | |
| B. | 反应后所得CO2的质量为40g | |
| C. | 参加反应的CO的质量为11.2g | |
| D. | 原混合物中CuO与Fe2O3的质量比为1:2 |
13.已知同温、同压下任何气体含有相同的分子数.现在有CO、CO2、O2混合气体9mL,在密闭容器中点火爆炸后恢复到原来状态,体积减少了1mL,再通过足量的NaOH溶液后又减少了5mL,则原来混合气体中CO、CO2、O2的体积比可能为( )
| A. | 2:1:6 | B. | 4:2:3 | C. | 5:3:1 | D. | 2:4:3 |
10.碳酸钠和碳酸氢钠是生活中常见的盐,通过实验验证、探究它们的化学性质.
【查阅资料】①Na2CO3+CaCl2=CaCO3↓+2NaCl ②2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O
③Ca(HCO3)2 易溶于水.
④CaCl2 溶液分别与 NaHCO3、Na2CO3 溶液等体积混合现象(表中的百分数为溶液中溶质的质量分数):
【进行实验】
【解释与结论】
(1)实验1中,NaHCO3与盐酸反应的化学方程式为NaHCO3+HCl═NaCl+H2O+CO2↑.
(2)实验2中,试剂a为澄清的石灰水.
(3)实验3中,NaHCO3与 CaCl2 反应的化学方程式为:2NaHCO3+CaCl2=CaCO3↓+2NaCl+CO2↑+H2O.
【反思与评价】
(1)实验2中,加热NaHCO3后,试管Ⅰ中残留固体成分可能为Na2CO3;Na2CO3,NaHCO3(写出所有可能).
(2)资料④中,NaHCO3 溶液与 CaCl2溶液混合的现象中,有些只观察到浑浊、未观察到气泡,原因可能是CaCl2溶液的溶质质量分数较小,生成的CO2量较少,CO2溶于水,因此没有气泡.
(3)用2种不同的方法鉴别 Na2CO3和NaHCO3固体,实验方案分别为:
①各取少量0.1%的NaHCO3和Na2CO3加入等质量的5%的CaCl2溶液,若无明显现象,则为NaHCO3,若观察到浑浊则为Na2CO3
②各取少量Na2CO3和NaHCO3固体于实验2装置中,分别加热一段时间,若观察到澄清石灰水变浑浊,固体为NaHCO3,若观察到无明显现象,固体为Na2CO3.
【查阅资料】①Na2CO3+CaCl2=CaCO3↓+2NaCl ②2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O
| NaHCO3 | Na2CO3 | ||||
| 0.1% | 1% | 5% | 0.1% | ||
CaCl2 | 0.1% | 无明显现象 | 有浑浊 | 有浑浊 | 有浑浊 |
| 1% | 无明显现象 | 有浑浊 | 有浑浊,有微小气泡 | 有沉淀 | |
| 5% | 无明显现象 | 有浑浊 | 有浑浊,有大量气泡 | 有沉淀 | |
④CaCl2 溶液分别与 NaHCO3、Na2CO3 溶液等体积混合现象(表中的百分数为溶液中溶质的质量分数):
【进行实验】
| 序号 | 实验装置 | 主要实验步骤 | 实验现象 |
| 实验 1 |  | 向2支试管中分别加入少 量Na2CO3和 NaHCO3溶液,再分别滴加盐酸 | 2支试管中均有气泡产生 |
| 实验 2 | 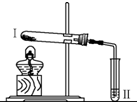 | 向Ⅱ中加入试剂 a,向Ⅰ中 加入少量 Na2CO3 或 NaHCO3 固体,分别加热一 段时间 | Na2CO3 受热时Ⅱ中无明 显现象; NaHCO3 受热时Ⅱ中出现 浑浊 |
| 实验 3 |  | 向Ⅱ中加入试剂 a,向Ⅰ中 加入少量 5%的 NaHCO3 溶 液,再滴加 5%的 CaCl2 溶 液 | Ⅰ中出现浑浊,有气泡产 生Ⅱ中出现浑浊 |
(1)实验1中,NaHCO3与盐酸反应的化学方程式为NaHCO3+HCl═NaCl+H2O+CO2↑.
(2)实验2中,试剂a为澄清的石灰水.
(3)实验3中,NaHCO3与 CaCl2 反应的化学方程式为:2NaHCO3+CaCl2=CaCO3↓+2NaCl+CO2↑+H2O.
【反思与评价】
(1)实验2中,加热NaHCO3后,试管Ⅰ中残留固体成分可能为Na2CO3;Na2CO3,NaHCO3(写出所有可能).
(2)资料④中,NaHCO3 溶液与 CaCl2溶液混合的现象中,有些只观察到浑浊、未观察到气泡,原因可能是CaCl2溶液的溶质质量分数较小,生成的CO2量较少,CO2溶于水,因此没有气泡.
(3)用2种不同的方法鉴别 Na2CO3和NaHCO3固体,实验方案分别为:
①各取少量0.1%的NaHCO3和Na2CO3加入等质量的5%的CaCl2溶液,若无明显现象,则为NaHCO3,若观察到浑浊则为Na2CO3
②各取少量Na2CO3和NaHCO3固体于实验2装置中,分别加热一段时间,若观察到澄清石灰水变浑浊,固体为NaHCO3,若观察到无明显现象,固体为Na2CO3.
14.以下发电过程中主要利用了化学变化的是( )
| A. | 风力发电 | B. | 水力发电 | C. | 火力发电 | D. | 太阳能发电 |
11.下列灭火方法及原理均正确的是( )
| A. | 家里油锅着火──锅盖盖灭──隔绝空气 | |
| B. | 废纸篓着火──用水浇灭──降低燃烧物的着火点 | |
| C. | 电器着火──立即用湿棉被盖灭──隔绝空气 | |
| D. | 酒精在桌上燃烧──用水浇灭──降低温度至可燃物着火点以下 |