题目内容
6.分别选用一种方法或试剂除去下列物质中的杂质(括号内的为杂质).(1)CO2(CO)通过灼热的氧化铜.
(2)生石灰(碳酸钙)高温煅烧.
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:(1)一氧化碳能与灼热的氧化铜粉末反应生成铜和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则.
(2)碳酸钙固体高温煅烧生成氧化钙和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则.
故答案为:(1)通过灼热的氧化铜;(2)高温煅烧.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.下列实验现象的描述中,不正确的是( )
| A. | 硫在空气中燃烧,产生刺激性气味的气体 | |
| B. | 在点燃的蜡烛火焰上压一块白瓷板,白瓷板上有黑色烟点 | |
| C. | 氢气在空气中燃烧发出淡蓝色火焰 | |
| D. | 木炭在氧气中燃烧,发出白光,生成二氧化碳 |
11.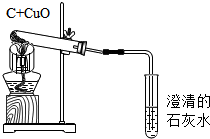 学习碳单质的性质时,某校实验小组的同学为探究碳的化学性质,按如下实验装置对木炭与氧化铜的反应进行实验探究.请你完成下列问题.
学习碳单质的性质时,某校实验小组的同学为探究碳的化学性质,按如下实验装置对木炭与氧化铜的反应进行实验探究.请你完成下列问题.
(1)实验目的:探究木炭是否具有还原性.
(2)实验用品:仪器:酒精灯,试管,铁架台.药品:木炭,氧化铜,澄清石灰水.
(3)实验中酒精灯加网罩的作用是提高温度.
(4)
(5)结论:木炭具有还原性.
(6)碳和氧化铜反应生成铜和二氧化碳.现有碳和氧化铜的混合物20g,高温加热混合物一段时间后,产生4.4g二氧化碳.求混合物中氧化铜的质量分数.
 学习碳单质的性质时,某校实验小组的同学为探究碳的化学性质,按如下实验装置对木炭与氧化铜的反应进行实验探究.请你完成下列问题.
学习碳单质的性质时,某校实验小组的同学为探究碳的化学性质,按如下实验装置对木炭与氧化铜的反应进行实验探究.请你完成下列问题.(1)实验目的:探究木炭是否具有还原性.
(2)实验用品:仪器:酒精灯,试管,铁架台.药品:木炭,氧化铜,澄清石灰水.
(3)实验中酒精灯加网罩的作用是提高温度.
(4)
| 实验现象 | 原因分析 |
| ① | |
| ② |
(6)碳和氧化铜反应生成铜和二氧化碳.现有碳和氧化铜的混合物20g,高温加热混合物一段时间后,产生4.4g二氧化碳.求混合物中氧化铜的质量分数.
15.我们在各大商场总能看到“金灿灿”的金制饰品,如戒指、项链、手链等.消费者在试戴时,售货员会提醒消费者,要轻轻地拉动,防止变形.据此不能得出的是( )
| A. | 金的熔点较高 | B. | 金的硬度较小 | ||
| C. | 金具有良好的延展性 | D. | 金的颜色为金黄色 |
16.下列物质属于纯净物的是( )
| A. | 不锈钢 | B. | 净化后的空气 | ||
| C. | 蒸馏水 | D. | 高锰酸钾完全分解后的剩余物 |