题目内容
5.人类的生产和生活都离不开金属及金属矿物,请回答下列问题:(1)铁锅长时间使用后易生锈,实际上是铁与空气中的水和氧气共同作用的结果,除去铁锈的方法是用砂纸擦或用稀酸洗或用除锈剂清洗等.
(2)炼铁的实验中,Fe2O3中的氧被CO夺去,铁被还原出来,CO是还原剂,在铁路建设中,长用铝和氧化铁反应生成铁单质对钢轨中的缝隙进行焊接,反应的化学方程式为:Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$X+2Fe,则X的化学式为Al2O3,该反应中的还原剂是铝.
(3)合成氨工业生产中所用的催化剂是铁触媒,其主要成分是FeO和Fe2O3,当FeO和Fe2O3中铁元素质量比为1:2时该催化剂的催化效果最好,此时FeO和Fe2O3的质量比为9:20(最简比).
分析 (1)根据铁生锈的条件及除去铁锈的方法解答;
(2)根据质量守恒定律中反应前后原子的种类及个数不变,可推知X的化学式;
(3)根据当FeO、Fe2O3中铁元素的质量比为1﹕2时,此时FeO、Fe2O3的质量比就等于二者的相对分子质量之比进行解答.
解答 解:
(1)铁锅长时间使用后易生锈,实际上是铁与与空气中的 水和氧气同时接触的结果;除去铁锈的方法是用砂纸擦或用稀酸洗或用除锈剂清洗等;
(2)据质量守恒定律中反应前后原子的种类及个数不变,反应前有2个铁原子、3个氧原子、2个铝原子,反应后除X外,有2个铁原子,因此可推知X的化学式为:Al2O3;由化学方程式可知,铝在反应中得到了氧,发生了氧化反应,是还原剂;
(3)当FeO、Fe2O3中铁元素的质量比为1:2时,此时FeO、Fe2O3的质量比就等于二者的相对分子质量之比,所以FeO、Fe2O3的质量比为(56+16):(56×2+16×3)=9:20.
答案:
(1)水和氧气;用砂纸擦或用稀酸洗或用除锈剂清洗等;
(2)Al2O3;铝;
(3)9:20
点评 本题主要考查了质量守恒定律的应用方面的知识和基本反应类型的判断,培养学生分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.下列图象能正确反映对应变化关系的是( )
| A. |  等质量的锌片、铝片分别与足量且质量分数相同的稀硫酸反应 | |
| B. |  向H2SO4和CuSO4的混合溶液中滴加NaOH溶液 | |
| C. |  定量的稀硫酸与锌片反应 | |
| D. |  向氢氧化钠溶液中不断加水,溶液的pH于加入水的质量关系 |
16.对联是中国传统文化的瑰宝之一,下列对联中单从字面意义看包含化学变化的是( )
| A. | 上联:冰冻兵船 兵打冰 冰开兵出 下联:尼姑泥鞋 尼洗泥 泥落尼归 | |
| B. | 上联:此木为柴山山出 下联:因火成烟夕夕多 | |
| C. | 上联:水陆洲 洲停舟 舟行洲不行 下联:天心阁 阁落鸽 鸽飞阁未飞 | |
| D. | 上联:水中冻冰 冰种雪 雪上加霜 下联:空中腾雾 雾成云 云开见日 |
13.下列变化属于化学变化的是( )
| A. | 酸雨腐蚀建筑物 | B. | 太阳能电池发电 | C. | 酒精挥发 | D. | 水的 天然循环 |
20.如图为a、b、c三种固体物质的溶解度曲线,下列说法中,正确的是( )


| A. | 将t2℃的a、b、c的饱和溶液降温到t1℃,溶液中溶质质量分数的关系是b>a=c | |
| B. | 当a混有少量b时,可用蒸发结晶的方法提纯a | |
| C. | t2℃时,a溶液的溶质质量分数一定大于b溶液的溶质质量分数 | |
| D. | t1℃时,分别将11g的a、b、c溶于50g的水中,所得溶液的溶质质量分数最大的是b |
10.根据下列粒子结构示意图所获取的信息,正确的是( )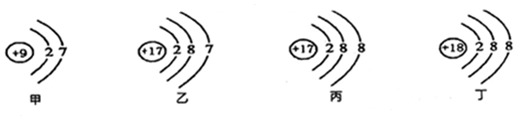

| A. | 甲、乙的化学性质相似 | B. | 乙、丙属于同种元素 | ||
| C. | 丙表示的是阳离子 | D. | 丁表示的元素属于金属元素 |
17.将足量的石灰石样品(主要成分是碳酸钙,所含杂质不溶于水,也不与其他物质反应),加入到盛有100g稀盐酸的烧杯中,立即将烧杯放在天平上称量.在以后的8分钟内,每一分钟读一次数.结果如下:
(1)表中有一个结果是不合理的,该结果的测得时间是第6分钟;
(2)根据上述数据,除了可以计算出生成的二氧化碳的质量是4.4g外,还能计算出以下结果的是BC(填序号)
A、石灰石样品中碳酸钙的质量分数
B、反应后所得不饱和溶液的溶质质量分数
C、参加反应的稀盐酸的溶质质量分数
(3)写出你的第(2)小题所选项的具体计算过程(如果有多个选项,请任选一项进行计算,计算结果精确到0.1%).
| 时间/分钟 | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 质量/g | 200.0 | 198.2 | 197.0 | 196.2 | 195.6 | 195.6 | 196 | 195.6 | 195.6 |
(2)根据上述数据,除了可以计算出生成的二氧化碳的质量是4.4g外,还能计算出以下结果的是BC(填序号)
A、石灰石样品中碳酸钙的质量分数
B、反应后所得不饱和溶液的溶质质量分数
C、参加反应的稀盐酸的溶质质量分数
(3)写出你的第(2)小题所选项的具体计算过程(如果有多个选项,请任选一项进行计算,计算结果精确到0.1%).
15.下列诗句 或名著事件的描述中既隐含物理变化又有化学变化的是( )
| A. | 伐薪烧炭南山中 | B. | 陆虞侯火烧草料场 | ||
| C. | 白玉为床金做马 | D. | 千里冰封,万里雪飘 |