题目内容
19.相同质量的镁、锌、铁三种金属,分别与足量的稀硫酸反应,产生氢气( )| A. | 镁最多 | B. | 锌最多 | C. | 铁最多 | D. | 一样多 |
分析 根据金属与酸反应生成氢气的质量与金属的相对原子质量和金属与酸反应生成盐的化合价有关进行分析.
解答 解:假设金属为一能够反应且化合价为+2价的金属M,其相对原子质量为x,金属的质量为m,生成的氢气的质量为y.
M+H2SO4=MSO4+H2↑
x 2
m y
$\frac{x}{2}$=$\frac{m}{y}$,y=$\frac{2m}{x}$,
通过这个式子可以看出,当等质量的金属完全反应时,生成的氢气的质量与金属的相对原子质量成反比,相对原子质量越大,生成的氢气的质量也就越小,质量相同的Mg、Fe、Zn分别与足量的稀硫酸反应,产生氢气的质量镁最多,锌最少.
故选:A.
点评 本题考查了金属与酸反应产生氢气质量的关系,完成此题,可以依据学过的知识.所以要求同学们在平时的学习中加强基础知识的记忆和理解,以便能够灵活应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.粗盐提纯实验的部分操作如图所示,其中错误的是( )
| A. | 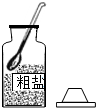 取一定量粗盐 | B. | 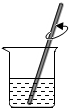 溶解 | C. | 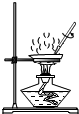 蒸发液体 | D. | 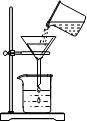 过滤 |
14.下列物质不属于合金的是( )
| A. | 黄铜 | B. | 青铜 | C. | 白铜 | D. | 紫铜 |
4.可以减少金属资源损失的有效措施之一是 ( )
| A. | 用塑料管代替铸铁管 | |
| B. | 用铝合金门窗代替铁窗框 | |
| C. | 化工厂周围设铁栅栏 | |
| D. | 停止生产使用所有金属材料的饮料罐 |