题目内容
13.甲、乙、丙三位同学通过调查,了解到某化工厂排放含有Zn2+、Hg2+、Fe3+、Cu2+四种金属离子的污水.为了从污水中回收金属铜,他们查阅有关资料(Fe+2FeCl3═3FeCl2;金属汞有剧毒,且具有挥发性),结合学过的化学知识,设计了三种方案(箭头线下的序号为实验步骤顺序).甲方案:
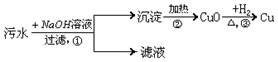
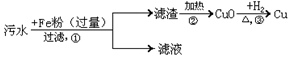
乙方案:
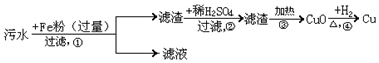
丙方案:
请根据他们的方案回答问题:
(1)三个实验方案中不能回收得到金属铜的是甲、丙方案.
(2)在能回收得到铜的方案中,哪一步操作应该采取什么措施防止空气污染?
分析 根据金属的性质以及物质间的反应、对环境的影响进行分析解答即可.
解答 解:甲方案中加入氢氧化钠,则会反应生成多种难溶性的碱,主要有氢氧化铜、氢氧化铁和氢氧化锌,加热都会生成相应的金属氧化物,故用氢气还原得不到纯净的铜;
乙的方案中,加入的是过量的铁,则铁会把汞和铜还原出来,过量的铁粉加入稀硫酸会反应掉,得到的滤渣加热,则汞会变成汞蒸气,剩余的氧化铜用氢气还原会得到铜,但是会污染环境;需要在步骤③进行连接冷凝装置使汞蒸气冷却;
丙的实验方案中,加入过量的铁粉,则得到的滤渣中含有铁以及生成的铜和汞,加热则汞会变成汞蒸气,但是滤渣中的铁除不去,故不能得到纯净的铜;
故答案为:(1)甲、丙;
(2)在步骤③进行连接冷凝装置使汞蒸气冷却.
点评 本题考查的是物质制备的知识,完成此题,可以依据已有的物质的性质进行.

练习册系列答案
相关题目
4.2010年“世界水日”的主题是“跨界水--共享的水、共享的机遇”.下列涉及水的变化中没有化学变化的是( )
| A. | 海水晒盐 | B. | 太阳能光解水制氢气 | ||
| C. | 饮用水生产时用ClO2消毒 | D. | 水作为原料参与植物光合作用 |
1.如图是a、b、c三种固体物质的溶解度曲线.下列说法中不正确的是( )
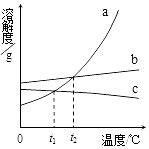

| A. | 在t2℃时,a的溶解度等于b的溶解度 | |
| B. | 在t1℃时,a、c饱和溶液中溶质的质量分数相同 | |
| C. | c的饱和溶液由t1℃升温至t2℃时,变成不饱和溶液 | |
| D. | 当a中含有少量b时,可以用降温结晶的方法提纯a |
8.2010年冬奥会兴奋剂检测是对运动员的一项重要检验.其中一种兴奋剂的化学式为C20H26O2,下列关于该兴奋剂的说法正确的是( )
| A. | 将该兴奋剂在足量的氧气中充分燃烧,产物为CO2和H2O | |
| B. | 该兴奋剂是由多原子构成的无机化合物 | |
| C. | 该兴奋剂是由20个碳原子、26个氢原子和2个氧原子构成 | |
| D. | 该兴奋剂中碳、氢、氧三种元素的质量比为20:26:2 |
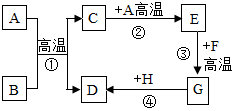 A-H都是常见的物质.已知B为黑色固体,D为红色固体单质,F为红色固体,H为蓝色的溶液.他们的转化关系如图所示.请回答:
A-H都是常见的物质.已知B为黑色固体,D为红色固体单质,F为红色固体,H为蓝色的溶液.他们的转化关系如图所示.请回答: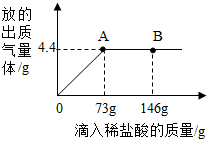 在一烧杯中盛有22.3克碳酸钠和氯化钠组成的固体混合物,向其中逐渐滴加溶质质量分数为10%的稀盐酸(Na2CO3+2HCl=2NaCl+H2O+CO2↑),放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示.请根据题意回答问题:
在一烧杯中盛有22.3克碳酸钠和氯化钠组成的固体混合物,向其中逐渐滴加溶质质量分数为10%的稀盐酸(Na2CO3+2HCl=2NaCl+H2O+CO2↑),放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示.请根据题意回答问题: