题目内容
19.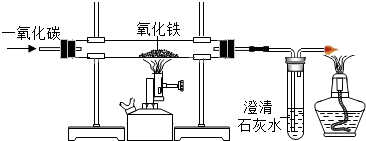 如图是实验室用CO还原Fe2O3的实验装置图,请完成下列各题;
如图是实验室用CO还原Fe2O3的实验装置图,请完成下列各题;(1)硬质玻璃管A中的实验现象固体由红棕色变成黑色,化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;试剂瓶B中实验现象澄清的石灰水变浑浊,化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O.
(2)实验开始时,要先通一会CO再加热,其目的是排净试管内的原有,空气防止爆炸.
(3)C处酒精灯的作用是点燃一氧化碳气体,防止污染空气.
分析 (1)根据实验验中发生的反应,分析实验的现象写化学方程式;
(2)根基实验的过程和注意的事项分析;
(3)根据实验的目的分析酒精灯的作用.
解答 解:(1)在加热的条件下,在硬质玻璃管中,一氧化碳与氧化铁反应生成了铁和二氧化碳,所以,反应的现象是:硬质玻璃管中固体由红棕色变成黑色;高温下一氧化碳和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;反应生成的二氧化碳与澄清的石灰水反应生成了碳酸钙沉淀和水,所以,实验的现象是:澄清的石灰水变浑浊,化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O;
(2)一氧化碳具有可燃性,必须注意纯度;先通一会CO再加热的原因是排净试管内的原有空气,防止爆炸;
(3)实验中左边的酒精灯加热玻璃管;右边的酒精灯:点燃一氧化碳气体,防止污染空气;
故答为:(1)硬质玻璃管中固体由红棕色变成黑色,Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;澄清的石灰水变浑浊,CO2+Ca(OH)2═CaCO3↓+H2O;
(2)排净试管内的原有,空气防止爆炸;(3)点燃一氧化碳气体,防止污染空气.
点评 本题考查了一氧化碳还原氧化铁的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
19.某些人睡觉常常磨牙是因为缺锌,这里的“锌”是指( )
| A. | 元素 | B. | 原子 | C. | 分子 | D. | 阴离子 |
10.下列变化属于物理变化的是( )
| A. | 煤气燃烧 | B. | 菜刀生锈 | C. | 牛奶变质 | D. | 瓷碗破碎 |
7.某化学兴趣小组在做完制取二氧化碳的实验后(用石灰石与稀盐酸制取),对反应后反应器中剩余溶液的溶质成分产生了兴趣,他们继续进行了如下实验探究.
【分析推断】根据制取二氧化碳的反应原理,可以确定剩余溶液中一定含有氯化钙,但其中是否含有氯化氢需要通过实验来证明.若剩余溶液显酸性(含有H+),说明含有氯化氢.
【查阅资料】碳酸钙不溶水,氢氧化钙微溶于水,氯化钙溶液显中性.
【实验过程】将剩余溶液倒入烧杯中,微热后冷却至室温.
【分析推断】根据制取二氧化碳的反应原理,可以确定剩余溶液中一定含有氯化钙,但其中是否含有氯化氢需要通过实验来证明.若剩余溶液显酸性(含有H+),说明含有氯化氢.
【查阅资料】碳酸钙不溶水,氢氧化钙微溶于水,氯化钙溶液显中性.
【实验过程】将剩余溶液倒入烧杯中,微热后冷却至室温.
| 实验操作 | 实验现象 | 实验结论 | |
| 甲同学 | 取烧杯中溶液少许于试管中,向其中滴加紫色石蕊试液 | 现象:溶液变红色 | 溶液显酸性(含有H+),溶质中有氯化氢 |
| 乙同学 | 取烧杯中溶液少许于试管中,向其中加入少量锌粒 | 现象:①锌粒逐渐溶解,有气泡产生 反应的化学方程式② Zn+2HCl=ZnCl2+H2↑ | |
| 丙同学 | 取烧杯中溶液少许于试管中,向其中加入少量石灰石 | 现象③石灰石逐渐溶解,有气泡产生 |
4.下列有关环境和能源的连线,前后关系不正确的是( )
| A. | 过量排放CO2-形成酸雨 | B. | 减少氟利昂的使用-防止臭氧空洞 | ||
| C. | 发展太阳能-开发清洁能源 | D. | 禁止滥砍乱发树木-减缓温室效应 |
11.下列说法错误的是( )
| A. | 二氧化碳易溶于水 | B. | 二氧化碳能使石蕊变红 | ||
| C. | 二氧化碳密度比空气大 | D. | 二氧化碳有毒不能供给呼吸 |
8.欲证明生石灰中含有未烧透的石灰石,最简单的方法是( )
| A. | 滴加足量稀盐酸 | B. | 加水溶解 | C. | 加入碳酸钠溶液 | D. | 高温煅烧 |
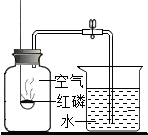 如图是小明测定空气中氧气含量的装置图,
如图是小明测定空气中氧气含量的装置图,