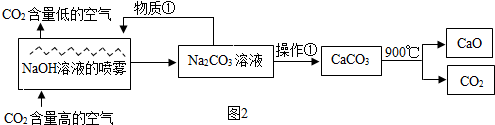
题目内容
4.金属铝及其合金有广泛的用途.(1)请画出铝的原子结构示意图;
(2)铝的化学性质活泼却耐腐蚀的原因;
(3)铝是两性金属,既可以与酸溶液反应,也可以与碱溶液反应,与NaOH溶液反应生成NaAlO2和H2.写出化学反应方程式;
(4)Al在高温条件下可以与Fe3O4发生置换反应,得到Fe与另一种氧化物,写出化学方程式;
(5)实验室制取某气体所需装置如图所示:
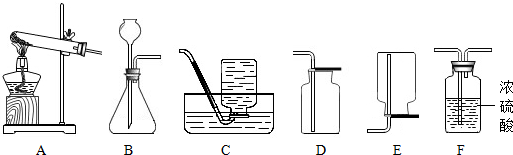
现欲制取一瓶干燥的H2,可选用图中的BFE组合制得.此操作中的发生装置还可以制取少量的另一种气体,请你写出产生另一种气体的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.实验前都要检查装置的气密性,请在图中选择一个气体发生装置,简述其气密性的检验方法先从长颈漏斗中注入水,当水浸没其下端管口时,用止水夹夹住导气管上连接的胶皮管,保证此处不漏气;然后再加入少量的水,若停止加水后,长颈漏斗中的水面不再下降,则说明此装置气密性良好.
(6)合金的用途十分广泛.某化学小组欲测定黄铜片(铜锌合金)的组成,进行了如下实验:取黄铜片30g放入烧杯中,将100g稀硫酸分5次加入烧杯中,每次均充分反应后,测得剩余固体的质量记录如表.
| 次 数 | 1 | 2 | 3 | 4 | 5 |
| 加入稀硫酸质量/g | 20 | 20 | 20 | 20 | 20 |
| 剩余固体质量/g | 26.75 | 23.5 | 20.25 | 17 | 16.5 |
分析 (1)Al的原子序数为13,原子核外有3个电子层,最外层电子数为3;
(2)根据铝在常温下与空气中的氧气发生化学反应,使铝的表面生成了一层致密的氧化铝薄膜解答;
(3)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写;再根据反应特征确定反应类型.
(4)Al与四氧化三铁发生铝热反应生成氧化铝与Fe;
(5)根据实验室制取氢气的反应物是固体和液体,反应条件是常温,排水法收集的气体纯净,排空气法收集的气体干燥,氢气密度比空气小,锌和硫酸反应生成硫酸锌和氢气进行分析;据实验室用过氧化氢制取氧气的反应物是固体和液体,反应条件是常温解答;
(6)根据金属镁的质量求出稀硫酸的溶质的质量即可求出所加稀硫酸的溶质的质量分数进行解答.
解答 解:
(1)Al的原子序数为13,原子核外有3个电子层,最外层电子数为3,则原子结构示意图为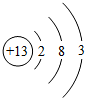 ;
;
(2)通常情况下铝制品很耐腐蚀,这是因为铝在常温下与空气中的氧气发生化学反应,使铝的表面生成了一层致密的氧化铝薄膜,从而阻止了内部的铝进一步氧化.
(3)Al与NaOH溶液反应生成H2和NaAlO2,反应的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
(4)Al与四氧化三铁发生铝热反应生成氧化铝与Fe,反应方程式为:8Al+3Fe3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Fe,
(5)实验室制取氢气的反应物是固体和液体,反应条件是常温,排水法收集的气体纯净,排空气法收集的气体干燥,浓硫酸进行干燥;氢气密度比空气小,所以应选用的装置组合是BFE;采取常温下二氧化锰催化分解过氧化氢溶液的方法,生成的氧气不易溶于不、密度大于空气;(或使用石灰石与稀盐酸反应,生成气体二氧化碳能溶于水);反应的化学方程式为2HCl+CaCO3═CaCl2+H2O+CO2↑(或2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑).
检验B装置的气密性的方法是:先从长颈漏斗中注入水,当水浸没其下端管口时,用止水夹夹住导气管上连接的胶皮管,保证此处不漏气;然后再加入少量的水,若停止加水后,长颈漏斗中的水面不再下降,则说明此装置气密性良好;
(6)与20g稀硫酸完全反应消耗锌的质量为:30g-26.75g=3.25g,
设与3.25g锌反应的硫酸的质量为x,
Zn+H2SO4=ZnSO4+H2↑,
65 98
3.25g x
$\frac{65}{3.25g}=\frac{98}{x}$
x=4.9g,
硫酸中溶质的质量分数为:$\frac{4.9g}{20g}×$100%=24.5%
答案:
(1)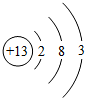 ;
;
(2)铝在常温下与空气中的氧气发生化学反应,使铝的表面生成了一层致密的氧化铝薄膜,从而阻止了内部的铝进一步氧化;
(3)2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
(4)8Al+3Fe3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Fe;
(5)AFE;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;先从长颈漏斗中注入水,当水浸没其下端管口时,用止水夹夹住导气管上连接的胶皮管,保证此处不漏气;然后再加入少量的水,若停止加水后,长颈漏斗中的水面不再下降,则说明此装置气密性良好;
(6)稀硫酸中溶质的质量分数为24.5%.
点评 本题主要考查了化学方程式的书写方法及其铝的性质和用途等方面的知识,可以依据已有的知识进行.

| A. | 属于氧化物 | |
| B. | 由两个金属元素和一个非金属元素组成 | |
| C. | 铁元素化合价为+6 | |
| D. | 其中钠、铁、氧元素质量比是2:1:4 |
| A. | KNO3 Na2CO3 KOH | B. | Na2SO4 FeCl3 NaCl | ||
| C. | HCl K2SO4 AgNO3 | D. | BaCl2 NH4Cl ZnSO4 |
| A. |  将质量相等且足量的锌粉和铁粉,分别投入相同质量、相同溶质质量分数的稀盐酸中 | |
| B. |  将一种稀硫酸均分成两份,分别向其中投入足量的氧化锌和碳酸锌 | |
| C. |  逐滴向一定量的氢氧化钠溶液中滴加稀盐酸直至过量 | |
| D. |  不断向稀盐酸和氯化铜的混合溶液中加入氢氧化钠溶液 |
 如图是炼铁的模拟实验示意图,该反应的化学方程式Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,下列有关说法错误的是( )
如图是炼铁的模拟实验示意图,该反应的化学方程式Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,下列有关说法错误的是( )| A. | 该实验可以观察到红色粉末变黑 | |
| B. | 待氧化铁完全反应,先停止通一氧化碳,后停止加热 | |
| C. | 氧化铁与一氧化碳的反应须在没有氧气的环境中进行 | |
| D. | 放置点燃的酒精灯目的是消除一氧化碳对环境的影响 |
| A. | 石灰石 | B. | 浓硫酸 | C. | 浓盐酸 | D. | 石灰水 |