题目内容
1.如图所示,1个甲分子与3个乙分子在一定条件下反应生成2个丙分子.则1个丙分子可表示为( )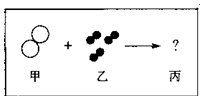
| A. |  | B. |  | C. | 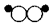 | D. |  |
分析 利用质量守恒定律的化学反应前后原子的种类与个数不变的知识解决.
解答 解:因为化学反应前后原子的种类与个数不变,由于反应前是“1个甲分子与3个乙分子”,所以在一定条件下反应生成2个丙分子,反应后产物中应存在2个甲分子中的原子,6个乙分子中的原子,故1个丙分子中原子的个数应含有甲分子中的1个原子和乙分子中的3个原子.
故选A.
点评 此题是一道反应图示题的考查,解题的关键是质量守恒定律的具体应用,以及相关的识图能力.

练习册系列答案
相关题目
9.甲、乙、丙三种物质在不同温度下的溶解度见下表:
下列有关说法正确的是( )
| 0℃ | 30℃ | 60℃ | 90℃ | |
| 甲 | 13.3克 | 45.8克 | 110克 | 202克 |
| 乙 | 35.5克 | 36.0克 | 37.1克 | 38.1克 |
| 丙 | 0.18克 | 0.16克 | 0.12克 | 0.08克 |
| A. | 降低温度可使丙的不饱和溶液变为饱和溶液 | |
| B. | 甲、乙、丙三种物质的溶解度大小顺序是甲>乙>丙 | |
| C. | 0℃时,三种物质的饱和溶液溶质质量分数甲>乙>丙 | |
| D. | 使乙物质从一定温度下的饱和溶液中析出,一般采用蒸发溶剂的方法 |
6.在制取CO2的实验中,小科发现质量相同而粗细不同的大理石与盐酸反应,CO2的产生速度细的比粗的快得多.经思考后,小科设计了如下实验(每次实验均用1g大理石,20mL盐酸)
(1)为了比较反应速度,设计如图一所示装置,其中量筒的作用是通过观察单位时间内排入量筒中水的体积来判断反应速率;
(2)实验中CO2体积随时间的变化关系如图二所示,请将实验2中CO2体积随时间变化的曲线画在图二中.
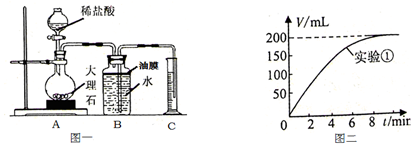
(3)已知20℃该气压下CO2气体密度约1.98g/L,求大理石中CaCO3的质量分数?
| 实验序号 | 温度(℃) | 大理石颗粒 | 盐酸质量分数(%) | 实验目的 |
| 1 | 20 | 粗 | 5 | 探究大理石和盐酸的反应速度与石灰石颗粒大小的关系 |
| 2 | 20 | 细 | 5 |
(2)实验中CO2体积随时间的变化关系如图二所示,请将实验2中CO2体积随时间变化的曲线画在图二中.

(3)已知20℃该气压下CO2气体密度约1.98g/L,求大理石中CaCO3的质量分数?
13.下列关于水资源的叙述,正确的是( )
| A. | 通常所说的水资源是指陆地上的所有水体 | |
| B. | 冰川分布于两极和高山地区,是目前可供人类利用的最重要的水资源之一 | |
| C. | 目前你用的淡水资源,主要是指河流水、湖泊淡水河浅层地下水 | |
| D. | 水资源开发利用后,都能很快恢复 |
10.物质的用途主要由其性质决定.下列物质的用途是利用其化学性质的是( )
| A. | 用氢氧化钠作干燥剂 | B. | 将氮气充入灯泡保护灯丝 | ||
| C. | 用活性炭消除房间的异味 | D. | 用干冰营造仙境般的舞台效果 |
11.下列属于纯净物的是( )
| A. | 稀硫酸 | B. | 钢 | C. | 五水合硫酸铜 | D. | 铁锈 |