题目内容
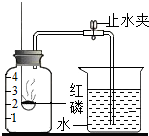 某同学设计了测定空气中氧气含量的实验,实验装置如图所示.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图所示.该同学的实验步骤如下:①将图中的集气瓶分为5等份,并做好标记.
②在燃烧匙内装入足量的红磷,将导管上的止水夹夹紧,在酒精灯上点燃红磷,并立即伸入集气瓶内,塞紧橡皮塞.
③充分反应后,待集气瓶冷却至室温,打开止水夹.
请回答下列问题:
(1)该实验中红磷需稍过量,目的是
(2)步骤③中打开止水夹后观察到的现象是
考点:空气组成的测定
专题:空气与水
分析:(1)为了将氧气充分消耗掉,应该保证红磷的量是过量的,可以据此解答该题;
(2))红磷燃烧消耗了广口瓶中的氧气而使瓶中压强小于外界大气压,而使烧杯中的水进入广口瓶中约占其体积的五分之一,可以据此解答该题;
(2))红磷燃烧消耗了广口瓶中的氧气而使瓶中压强小于外界大气压,而使烧杯中的水进入广口瓶中约占其体积的五分之一,可以据此解答该题;
解答:解:
(1)红磷燃烧产生了大量的白烟,生成了五氧化二磷固体,为了将氧气充分消耗掉,应该保证红磷的量是过量的;
(2)红磷与氧气反应生成固体,消耗了瓶内的气体,压强减小,外界大气压会把水进入集气瓶,约占集气瓶体积的
,故答案:水进入集气瓶内约占集气瓶体积的
,由此可粗略证明:空气中的氧气约占空气总体积的
.
答案:
(1)为了将氧气充分消耗掉;
(2)水进入集气瓶内约占集气瓶体积的
21%
(1)红磷燃烧产生了大量的白烟,生成了五氧化二磷固体,为了将氧气充分消耗掉,应该保证红磷的量是过量的;
(2)红磷与氧气反应生成固体,消耗了瓶内的气体,压强减小,外界大气压会把水进入集气瓶,约占集气瓶体积的
| 1 |
| 5 |
| 1 |
| 5 |
| 1 |
| 5 |
答案:
(1)为了将氧气充分消耗掉;
(2)水进入集气瓶内约占集气瓶体积的
| 1 |
| 5 |
点评:根据对空气组成成分的认识,利用镁的性质及题中资料信息,分析导致实验中所出现现象的可能性,考查获得信息解决问题的能力.

练习册系列答案
相关题目
在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前后各物质的质量分数如下表所示.下列说法正确的是( )
| 甲 | 乙 | 丙 | 丁 | |
| 反应前 | 70% | 14% | m | 10% |
| 反应后 | 42% | n | 40% | 10% |
| A、丙可能是单质 |
| B、甲、乙的质量之和一定等于生成丙的质量 |
| C、丁一定是该反应的催化剂 |
| D、若消耗3 g的乙,则生成17g的丙 |
氨碱法用食盐制纯碱的反应原理是:
(1)NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl (2)2NaHCO3
Na2CO3+H2O+CO2↑
下列对上述信息的有关理解中,错误的是( )
(1)NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl (2)2NaHCO3
| ||
下列对上述信息的有关理解中,错误的是( )
| A、用食盐制纯碱需要含碳、氧元素的物质 |
| B、在该条件下,NaHCO3的溶解度比NH4Cl小 |
| C、在反应(1)中析出固体后的溶液是NaHCO3 的不饱和溶液 |
| D、副产品氯化铵是一种盐 |
下列物质不属于单质的是( )
| A、水 | B、镁条 | C、硫粉 | D、液氮 |
 某兴趣小组的同学做如图所示的实验探究分子的运动,回答下列问题:
某兴趣小组的同学做如图所示的实验探究分子的运动,回答下列问题: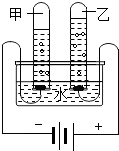 如图是电解水的装置.通电后两极上都有气体放出.根据电解水的实验,得出以下结论:
如图是电解水的装置.通电后两极上都有气体放出.根据电解水的实验,得出以下结论: