题目内容
20.下列图象能正确反映对应变化关系的是( )| A. | 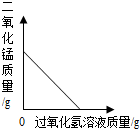 向一定量的二氧化锰中加入过氧化氢溶液 | |
| B. | 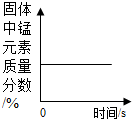 加热一定量的高锰酸钾固体 | |
| C. | 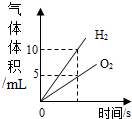 通直流电电解水一段时间 | |
| D. | 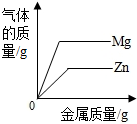 向两份完全相同的稀盐酸中分别加入足量的镁粉和锌粉 |
分析 A、二氧化锰在过氧化氢分解的过程中充当的是催化剂,可以结合催化剂的定义来完成解答;
B、高锰酸钾分解产生了氧气,所以反应前后锰元素的质量分数要改变,可以据此解答;
C、根据通电分解水的实验现象及结论进行解答.
D、根据氢元素的质量守恒来进行判断;
解答 解:A、二氧化锰在过氧化氢分解的过程中充当的是催化剂,其质量在反应前后不会改变,故A错误;
B、高锰酸钾分解产生了氧气,使固体的总质量减少,锰元素的质量不变,所以锰元素的质量分数增加,故B错误;
C、通电分解水时产生氢气的体积是氧气的二倍,故C正确.
D、向两份完全相同的稀盐酸中分别加入锌粉、镁粉,由于镁粉和锌粉是足量的,所以产生氢气质量应该相等,故D错误;
故选C.
点评 解答这类题目时,首先,要熟记实验室制取氧气的反应原理(即实验室制取氧气的文字表达式和化学方程式),各物质的颜色、状态,反应的条件、类型,以及实验室制取氧气的反应原理和发生装置的相互联系;并且,一定要理解催化剂的概念、催化作用;等等;然后,根据所给的问题情景及相关信息,结合所学的相关知识和技能,联系起来细心地探究、推理后,按照题目要求进行选择或解答即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.如图为某化学反应的微观示意图(▼◆○分别代表三种不同原子).下列说法错误的是( )


| A. | 分子在化学变化中可以再分 | |
| B. | 此反应生成物中有单质 | |
| C. | 原子在化学变化中不可再分 | |
| D. | 参加反应的两种分子的个数比为1:1 |
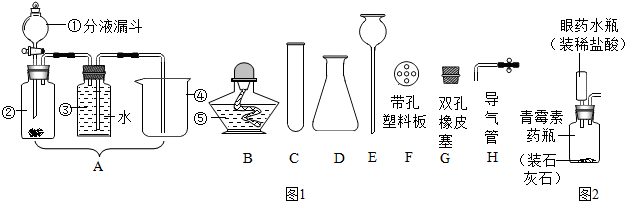
5.根据如图所示装置回答问题:

(1)写出下列仪器的名称:①试管②集气瓶.
(2)实验室若用B装置来制取二氧化碳,应往长颈漏斗中入稀盐酸,若用G装置来收集二氧化碳,二氧化碳应从a进入(选“a”或“b”).如果选择装置C制取二氧化碳,与B装置相比,其优点是:可以控制反应的发生和停止.
(3)用不加催化剂的方法制取氧气,选择的发生装置是A,反应的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;若选择G装置(事先装满水)收集氧气,则氧气应从b通入(选“a”或“b”).
(4)某化学兴趣小组欲测定一块石灰石样品中碳酸钙的质量分数(假设样品中的杂质不溶于水也不与盐酸反应).将15.0g石灰石样品放入烧杯中,再取100g稀盐酸分4次加入烧杯中,每次均充分反应.实验数据记录如下:
试计算:
①生成二氧化碳的总质量4.4g
②第1次加入稀盐酸充分反应后,烧杯中物质的总质量m为38.2
③该石灰石样品中碳酸钙的质量分数(写出计算过程).

(1)写出下列仪器的名称:①试管②集气瓶.
(2)实验室若用B装置来制取二氧化碳,应往长颈漏斗中入稀盐酸,若用G装置来收集二氧化碳,二氧化碳应从a进入(选“a”或“b”).如果选择装置C制取二氧化碳,与B装置相比,其优点是:可以控制反应的发生和停止.
(3)用不加催化剂的方法制取氧气,选择的发生装置是A,反应的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;若选择G装置(事先装满水)收集氧气,则氧气应从b通入(选“a”或“b”).
(4)某化学兴趣小组欲测定一块石灰石样品中碳酸钙的质量分数(假设样品中的杂质不溶于水也不与盐酸反应).将15.0g石灰石样品放入烧杯中,再取100g稀盐酸分4次加入烧杯中,每次均充分反应.实验数据记录如下:
| 次 数 | 第1次 | 第2次 | 第3次 | 第4次 |
| 加入稀盐酸质量/g | 25 | 25 | 25 | 25 |
| 反应后烧杯中物质的总质量/g | m | 61.4 | 85.6 | 110.6 |
①生成二氧化碳的总质量4.4g
②第1次加入稀盐酸充分反应后,烧杯中物质的总质量m为38.2
③该石灰石样品中碳酸钙的质量分数(写出计算过程).
9.下列各组物质的稀溶液,不用其他试剂就能鉴别出来的是( )
| A. | BaCl2、Na2SO4、Na2CO3、HCl | B. | KCl、AgNO3、HCl、HNO3 | ||
| C. | FeCl3、HCl、Ca(OH)2、NaOH | D. | Ba(OH)2、Na2SO4、CuCl2、MgCl2 |
10.某矿石在氧气中燃烧,反应的化学方程式是4X+11O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3+8SO2.下列有关说法中不正确的是( )
| A. | X的化学式是FeS2 | |
| B. | SO2中的硫、氧元素的质量比为1:2 | |
| C. | 反应前后氧元素的化合价发生改变 | |
| D. | Fe2O3中的铁氧、元素的原子个数比为2:3 |