题目内容
8. 钢铁是生产、生活中使用非常广泛的金属.
钢铁是生产、生活中使用非常广泛的金属.(1)铁锅可用来炒菜,利用了金属的传导热性.
(2)某企业仓库里长期堆放的机械设备的锈迹斑斑,其原因是铁长期与空气中水和氧气接触,发生了缓慢氧化所致.
(3)小明将设备上的一枚生锈的螺丝放入足量的稀硫酸中,发现铁锈逐渐消失,溶液变成黄色,一段时间后,又观察到铁钉表面有大量气泡产生,请写出溶液变黄的化学反应式Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
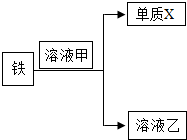
(4)为探究金属的化学性质,小明将处理后的铁钉放在溶液甲中继续实验(如图),下列说法错误的是D.
A、若X为非金属单质,则溶液甲可能是浓硫酸
B、若X为金属单质,则X的活动性一定比铁强
C、若溶液甲是硫酸镁溶液,则溶液乙的质量大于溶液甲的质量
D、若溶液甲是硝酸银和硝酸铜的混合溶液,则溶液乙可能只含有Cu2+和Fe2+两种阳离子.
分析 (1)根据铁的性质和用途分析回答;
(2)根据铁生锈的条件分析;
(3)根据氧化铁与硫酸的反应分析回答;
(4)根据金属活动性顺序表的应用分析回答.
解答 解:(1)铁锅可用来炒菜,利用了金属的导热性.
(2)某企业仓库里长期堆放的机械设备的锈迹斑斑,其原因是铁长期与空气中水和氧气接触,发生了缓慢氧化所致.
(3)小明将设备上的一枚生锈的螺丝放入足量的稀硫酸中,发现铁锈逐渐消失,溶液变成黄色,一段时间后,又观察到铁钉表面有大量气泡产生,溶液变黄的原因是氧化铁与硫酸反应生成了硫酸铁和水,化学反应式是:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
(4)A、由于浓硫酸具有强氧化性,与铁反应不能生成氢气,故A错误;
B、若X为金属单质,则X的活动性一定比铁若,故B错误;
C、若溶液甲是硫酸镁溶液,铁不与硫酸镁反应,则溶液质量不变.故C错误;
D、若溶液甲是硝酸银和硝酸铜的混合溶液,当硝酸银完全反应后,则溶液乙可能只含有Cu2+和Fe2+两种阳离子.故D正确.
故答为:(1)导热;(2)水和氧气;(3)Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;(4)D.
点评 本题的难度不大,了解金属的性质和应用的知识是解答本题的基础.

练习册系列答案
相关题目
19.下列图示的实验操作正确的是( )
| A. |  熄灭酒精灯 | B. |  取用碳酸钠固体 | C. | 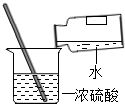 稀释浓硫酸 | D. | 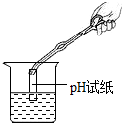 测溶液酸碱度 |
16. 兴趣小组的同学为研究酸和碱反应的特点,将稀盐酸匀速、缓慢地滴入盛有氢氧化钠溶液的烧杯中,并测绘出烧杯内溶液的温度和pH的变化图象(如图所示),请回答问题:
兴趣小组的同学为研究酸和碱反应的特点,将稀盐酸匀速、缓慢地滴入盛有氢氧化钠溶液的烧杯中,并测绘出烧杯内溶液的温度和pH的变化图象(如图所示),请回答问题:
(1)由pH变化图象可知,在t1时刻,烧杯中存在的阴离子是Cl-和OH-(填写离子符号).
(2)由温度变化图象可知,稀盐酸和氢氧化钠溶液发生的化学反应是放热(选填“放热”或“吸热”)反应.
(3)根据酸和碱反应的特点,可将氢氧化铝制成抗胃酸(主要成分为HCl)药剂,它与另一种抗胃酸药剂碳酸氢钠相比,在建议每次服用剂量下(见表),其药效“强”而且“持久”,其可能原因是:0.25g含Al(OH)3的抗胃酸药剂比0.5g含NaHCO3的抗胃酸药剂能中和更多的HCl,所以药效强于NaHCO3;Al(OH)3和HCl反应速率慢于NaHCO3和HCl,所以药效比服用NaHCO3持久.(提示:NaHCO3+HCl=NaCl+H2O+CO2↑)
 兴趣小组的同学为研究酸和碱反应的特点,将稀盐酸匀速、缓慢地滴入盛有氢氧化钠溶液的烧杯中,并测绘出烧杯内溶液的温度和pH的变化图象(如图所示),请回答问题:
兴趣小组的同学为研究酸和碱反应的特点,将稀盐酸匀速、缓慢地滴入盛有氢氧化钠溶液的烧杯中,并测绘出烧杯内溶液的温度和pH的变化图象(如图所示),请回答问题:(1)由pH变化图象可知,在t1时刻,烧杯中存在的阴离子是Cl-和OH-(填写离子符号).
(2)由温度变化图象可知,稀盐酸和氢氧化钠溶液发生的化学反应是放热(选填“放热”或“吸热”)反应.
(3)根据酸和碱反应的特点,可将氢氧化铝制成抗胃酸(主要成分为HCl)药剂,它与另一种抗胃酸药剂碳酸氢钠相比,在建议每次服用剂量下(见表),其药效“强”而且“持久”,其可能原因是:0.25g含Al(OH)3的抗胃酸药剂比0.5g含NaHCO3的抗胃酸药剂能中和更多的HCl,所以药效强于NaHCO3;Al(OH)3和HCl反应速率慢于NaHCO3和HCl,所以药效比服用NaHCO3持久.(提示:NaHCO3+HCl=NaCl+H2O+CO2↑)
| 主要成分 (均占药片质量的95%) | 主要成分的 相对分子质量 | 建议每次 服用剂量/g |
| Al(OH)3 | 78 | 0.25 |
| NaHCO3 | 84 | 0.5 |
18.根据某城市某日空气质量日报的部分内容,下列行为对对表中三个空气质量指数不会产生影响的是( )
| 项目 | 空气污染指数 | 空气质量级别 | 空气质量描述 |
| 总悬浮颗粒物 | 65 | Ⅱ | 良 |
| 二氧化硫(SO2) | 7 | ||
| 二氧化氮(NO2) | 24 |
| A. | 焚烧垃圾 | B. | 汽车排放尾气 | ||
| C. | 用煤和石油产品作燃料 | D. | 生活污水未经处理直接排放 |
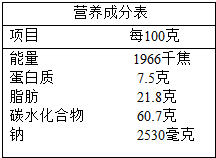 某方便面的营养成分表如图(其中碳水化合物主要指淀粉等):
某方便面的营养成分表如图(其中碳水化合物主要指淀粉等):
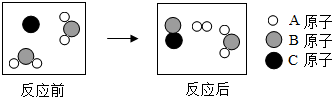 如图是某化学反应的微观示意图,该反应的基本类型是置换反应,生成物中A元素的化合价为0.
如图是某化学反应的微观示意图,该反应的基本类型是置换反应,生成物中A元素的化合价为0.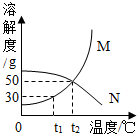 溶解度是解决溶液相关问题的重要依据,请根据如图溶解度曲线解决下列问题.
溶解度是解决溶液相关问题的重要依据,请根据如图溶解度曲线解决下列问题.