题目内容
海洋面积约占地球表面积的71%,海洋孕育了地球上的生命,又给这些生命提供丰富的资源.
Ⅰ.化工厂利用海水和贝壳(主要成分CaCO3)制取金属镁,流程如下:
(1)写出电解无水MgCl2时得到的另一种产物在生产生活中的用途 .(任写一种)
(2)分别写出①和④的化学方程式 、 .
Ⅱ.如图是超市销售的一种加点盐标签上的部分文字说明,碘元素是人体必须的 (填“常量”或微量:)元素,毎袋该食盐碘元素的质量为 mg,若成人每天需摄入碘元素0.15mg,仅靠这种加碘食盐获取则每天需食用这种食盐 g.

| 对海洋资源的合理开发与利用;金属的物理性质及用途;碱的化学性质;盐的化学性质;化合物中某元素的质量计算;标签上标示的物质成分及其含量;矿物质与微量元素 | |
| 专题: | 标签图示型;常见的盐 化学肥料. |
| 分析: | 根据已有的知识进行分析,电解氯化镁生成的氯气是制盐酸的主要原料;根据反应书写反应的化学方程式;根据标签进行有关的计算即可. |
|
| 解:Ⅰ(1)电解氯化镁生成的氯气是制盐酸的主要原料,故填:制盐酸; (2)碳酸钙高温能分解生成氧化钙和二氧化碳,氢氧化镁能和盐酸反应生成氯化镁和水,故填:CaCO3 Ⅱ碘元素是人体必须的微量元素; |
| 点评: | 本题考查了化学与生活的知识,完成此题,可以依据已有的知识结合题干提供的信息进行. |

 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案图中a、b、c分别表示KNO3、NaCl、Ca(OH)2溶解度曲线,下列说法错误的是( )

|
| A. | T1时,KNO3和NaCl的饱和溶液溶质的质量分数相等 |
|
| B. | T2时,A点表示KNO3的不饱和溶液,降温至T1时有晶体析出,且变为T1时KNO3的饱和溶液 |
|
| C. | T1时,将Ca(OH)2饱和溶液升温至T2变为不饱和溶液 |
|
| D. | 温度高于T1时,KNO3溶解度大于NaCl溶解度,温度低于T1时,KNO3溶解度小于NaCl溶解度 |
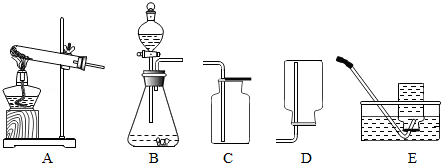
下列装置使用不恰当的是( )
|
| A. |
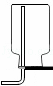
实验室收集氢气 | B. |
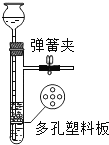
用现有条件检查装置气密性 |
|
| C. |
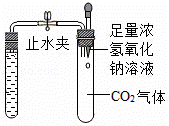
证明CO2能与NaOH溶液反应 | D. |
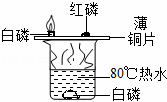
探究燃烧的三个条件 |
守恒思想是化学中重要的学科思想,电荷守恒便是其中之一,电荷守恒是指溶液中所有的阳离子所带正电荷之和等于所有阴离子所带负电荷之和.例如:某Na2SO4溶液中x个Na+,y个SO42﹣,则该溶液电荷守恒可表示为x=2y.现有一混合溶液,组成如下表所示:
| 离子 | K+ | Mg2+ | Cl﹣ | SO42﹣ |
| 个数 | a | b | c | d |
回答下列问题:
(1)该混合液的电荷守恒可表示为: (用a、b、c表示)
(2)若该溶液中有两种溶质,这两种溶质可以是KCl和MgSO4,也可以是 和 .
2013年3月在上海和安徽相继发现H7N9型禽流感,达菲是一种抗病毒药物,能有效防治H7N9型禽流感,其化学式为C16H28O4N2,下列有关说法不正确的是( )
|
| A. | 达菲由四种元素组成 |
|
| B. | 一个达菲分子由50个原子构成 |
|
| C. | 达菲中碳、氢、氧三种元素的质量之比为48:7:16 |
|
| D. | 达菲完全燃烧后只生成二氧化碳和水 |
我国著名的闽籍制碱专家侯德榜,在纯碱制造方面做出了重大贡献。用“侯氏制碱法”制得的纯碱中常含有氯化钠等杂质,化学兴趣小组欲对某品牌纯碱样品中碳酸钠的质量分数进行实验探究,在老师的指导下,他们设计了下列两种实验方案进行试验。
资料摘要:碱石灰常用于吸收水蒸气和二氧化碳。
[方案一] 样品与氯化钙溶液反应,测定Na2CO3的质量分数
(1)样品与氯化钙溶液的反应实验(杂质不与氯化钙溶液反应):
| 实验操作 | 实验现象 | 实验结论 |
| 取一定量纯碱样品配成溶液后,滴加足量的CaCl2溶液。 | 产生白色沉淀 | 反应的化学方程式: __________▲___________ |
(2)分析滴加的CaCl2溶液要足量的原因:__________▲_____________。
(3)将反应后的混合物进行过滤,把获得的沉淀物进行洗涤、干燥、称量。利用沉淀物质量计算Na2CO3的质量分数为91%。如果不洗涤沉淀物会造成测定结果大于91%,这是因为__________▲_____________。
[方案二] 样品与稀盐酸反应,测定Na2CO3的质量分数
利用下图所示实验装置(铁架台略去)和试剂,通过测定样品和稀盐酸反应产生的CO2气体的质量,计算Na2CO3的质量分数(装置气密性良好,忽略盐酸的挥发性且每步反应或作用都是完全的)。
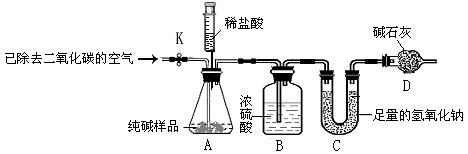
(4)打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,以排尽装置A和B中含有的__▲___,再接上装置C和D。
(5)关闭止水夹K,加入足量的稀盐酸(杂质不与盐酸反应)。待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入已除去CO2的空气一会儿,目的是__________▲__________。装置__▲__(填标号)在反应前后的质量差就是产生CO2的质量,由此计算出该样品中Na2CO3的质量分数。若没有装置D,将会使测定结果__▲__(选填“偏大”或“偏小”)。
(6)某纯碱样品中含有杂质NaCl,为测定该样品中Na2CO3的质量分数,称取纯碱样品 6 g,放入20 g水中使其完全溶解,再加入稀盐酸26.2 g,恰好完全反应,反应后溶液的总质量为50 g。试计算:①生成二氧化碳的质量;②样品中Na2CO3的质量分数。(写出计算过程,结果保留一位小数)
 解答:
解答: CaO+CO2↑,2HCl+Mg(OH)2═MgCl2+2H2O;
CaO+CO2↑,2HCl+Mg(OH)2═MgCl2+2H2O;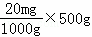 =10mg,成人每天需摄入碘元素0.15mg,仅靠这种加碘食盐获取则每天需食用这种食盐的质量为0.15mg
=10mg,成人每天需摄入碘元素0.15mg,仅靠这种加碘食盐获取则每天需食用这种食盐的质量为0.15mg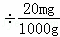 =7.5g,故填:微量,10,7.5.
=7.5g,故填:微量,10,7.5.