题目内容
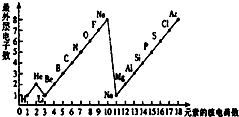 学完元素周期表以后,小明想探究一下1~18号元素的核电荷数和最外层电子数的关系,绘制了如图所示的关系图,请据图回答下列问题:
学完元素周期表以后,小明想探究一下1~18号元素的核电荷数和最外层电子数的关系,绘制了如图所示的关系图,请据图回答下列问题:(1)一个水分子(H2O)中共有
(2)一个Al3+核外共有
(3)通过绘制的图示,你能帮助小明发现哪些规律?请写出其中的二个:
①
②
考点:元素周期表的特点及其应用,原子和离子的相互转化
专题:化学用语和质量守恒定律
分析:(1)由图中1~18号元素原子最外层电子数与原子核电荷数的关系图可知:氢元素、氧元素的质子数;
(2)一个Mg2+是失去2个电子而带的正电荷,故可知其离子核外电子数;Cl-是得到1个电子而带的负电荷,故可知其离子最外层电子数;
(3)通过对该图的分析,总结归纳规律.
(2)一个Mg2+是失去2个电子而带的正电荷,故可知其离子核外电子数;Cl-是得到1个电子而带的负电荷,故可知其离子最外层电子数;
(3)通过对该图的分析,总结归纳规律.
解答:解:(1)根据“核内质子数=核外电子数=核电荷数”,由图中1~18号元素原子最外层电子数与原子核电荷数的关系图可知:氢元素、氧元素的质子数分别为:1、8;又因为1个水分子由2个氢原子和1个氧原子构成;故一个水分子共有3个原子核,1×2+8=10个质子;
(2)一个Mg2+是失去2个电子而带的正电荷,故可知其离子核外电子数为:12-2=10个;Cl-是得到1个电子而带的负电荷,故可知其离子最外层电子数为:7+1=8,故与Ar、Ne原子的最外层电子数相同;
(3)通过对该图的分析,总结归纳规律:随着核电荷数的递增,最外层电子数呈周期性变化;同一周期中的元素电子层数相同.
故答为:(1)3,10,10;(2)10,Ar;(3)随着核电荷数的递增,最外层电子数呈周期性变化;同一周期中的元素电子层数相同.
(2)一个Mg2+是失去2个电子而带的正电荷,故可知其离子核外电子数为:12-2=10个;Cl-是得到1个电子而带的负电荷,故可知其离子最外层电子数为:7+1=8,故与Ar、Ne原子的最外层电子数相同;
(3)通过对该图的分析,总结归纳规律:随着核电荷数的递增,最外层电子数呈周期性变化;同一周期中的元素电子层数相同.
故答为:(1)3,10,10;(2)10,Ar;(3)随着核电荷数的递增,最外层电子数呈周期性变化;同一周期中的元素电子层数相同.
点评:了解原子的定义和构成:原子由原子核和核外电子构成,其中原子核由质子和中子构成的;了解核外电子在化学反应中的作用.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
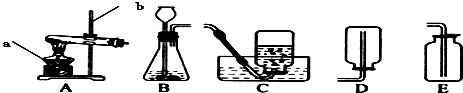
下列图示的化学实验操作错误的是( )
A、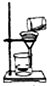 过滤 |
B、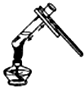 给液体加热 |
C、 检查装置的气密性 |
D、 稀释浓硫酸 |