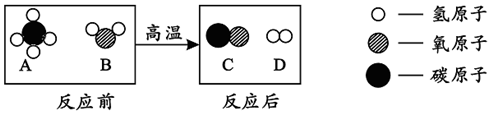
题目内容
14.如图装置有贮气、洗气等多种用途.以下有关该装置用途的说法正确的是( )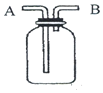
| A. | 用排空气法收集O2,气体从B管进 | |
| B. | 用于病人输氧,瓶内盛放水,B管接供氧钢瓶 | |
| C. | 测量CO2体积时,瓶内盛满水,气体从B管进,A管接量筒 | |
| D. | 除去H2中的H2O,瓶内盛放浓硫酸,气体从A管进 |
分析 该装置具有储气的功能:若瓶内是空气,收集比空气密度大的气体,可以从A进,从B出;收集比空气密度小的气体,可以B进A出;若瓶内是水,则可以收集不溶于水的气体,B进A出;
该装置具有洗气的功能:若干燥气体,里面可放的液体是具有吸水性的液体;若除去气体中的其他杂质(水蒸气除外),也可以放置能与杂质气体反应但不能与原气体反应的液体,气体都是A进B出.
解答 解:A、收集氧气时,氧气密度比空气密度大,要从A进B出能排出装置中的空气,故A说法错误;
B、用于病人输氧,瓶内盛放水,A管接供氧钢瓶,利用氧气不溶于水的性质,观察气泡的速度,从而确定出供氧的速度,故B说法错误;
C、CO2气体能溶于水,所以不能用排水法收集,故C说法错误;
D、该装置可以装入不同的试剂来除去气体中的杂质,这时气体都要长进短出,除去H2中的H2O,瓶内盛放浓硫酸,气体从A管进,故D说法正确.
故选:D.
点评 该题目考查对多用途装置的使用方法,了解各种不同气体的性质和装置的特点是解答问题的关键.

练习册系列答案
相关题目
4.为探究酸的化学性质,进行如图1实验:

①甲实验没有观察到明显现象,乙实验现象是产生气泡
②将反应后甲乙两试管中的溶液部分倒入烧杯中,没有观察到明显现象.
由此猜想反应后乙试管中溶液的溶质:
a.NaCl、HCl b.NaCl
③为了验证猜想a,某同学对乙试管中剩余溶液,设计了如下实验方案.
Ⅰ.方案2不合理的理由是NaCl+AgNO3=AgCl↓+NaNO3(用化学方程式表示).
Ⅱ.下列物质代替石蕊试液,也可以达到验证目的,其中不正确的是D(填序号).
A.铁粉 B.碳酸钠粉末 C.氧化铜粉末 D.氢氧化钠
④利用酸的性质测定锌铜混合物中铜的质量分数.取10g样品置于烧杯中,加入一定质量的稀硫酸.所加稀硫酸与生成气体的质量关系如图2所示.
Ⅰ.氢气的物质的量是0.1mol.
Ⅱ.求该样品中铜的质量分数.(利用化学方程式计算)

①甲实验没有观察到明显现象,乙实验现象是产生气泡
②将反应后甲乙两试管中的溶液部分倒入烧杯中,没有观察到明显现象.
由此猜想反应后乙试管中溶液的溶质:
a.NaCl、HCl b.NaCl
③为了验证猜想a,某同学对乙试管中剩余溶液,设计了如下实验方案.
| 方案编号 | 实验操作 | 实验现象 | 结论 |
| 方案1 | 取样于试管中,滴加紫色石蕊试液 | 溶液变红色 | 猜想a成立 |
| 方案2 | 取样于试管中,滴加硝酸银溶液 | 产生白色沉淀 |
Ⅱ.下列物质代替石蕊试液,也可以达到验证目的,其中不正确的是D(填序号).
A.铁粉 B.碳酸钠粉末 C.氧化铜粉末 D.氢氧化钠
④利用酸的性质测定锌铜混合物中铜的质量分数.取10g样品置于烧杯中,加入一定质量的稀硫酸.所加稀硫酸与生成气体的质量关系如图2所示.
Ⅰ.氢气的物质的量是0.1mol.
Ⅱ.求该样品中铜的质量分数.(利用化学方程式计算)
9.下列化学用语书写正确的是( )
| A. | 三个钾原子:3K+ | B. | 镁离子:Mg+2 | C. | 两个银原子:2Ag | D. | 铝元素:AL |
6.2015年中国科学家屠呦呦因青蒿索(C15H22O5)和双氢青蒿素(C15H24O5)而荣获了诺贝尔奖.下列有关说法中不正确的是( )
| A. | 青蒿素比双氢青蒿素少两个氢原子 | |
| B. | 青蒿素中C、H、O三种元素的质量比是90:11:40 | |
| C. | 青蒿素和双氢青蒿索分子中碳、氧原子个数比都为3:1 | |
| D. | 青蒿素中氧元素的质量分数比双氢青蒿素中氧元素的质量分数大 |
3.下列有关碳及其化合物描述不正确的是( )
| A. | 清朝的碳素字画能长久保存的原因是碳在常温下化学性质不活泼 | |
| B. | 在一定条件下CO和CO2可以相互转化 | |
| C. | CO和CO2都会导致动物死亡是因为它们具有毒性 | |
| D. | 碳和一氧化碳都可以用来还原氧化铜 |
4. 已知
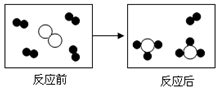
已知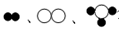 分别表示X、Y、Z三种不同的气体分子,其在一定条件下的变化如图所示,通过图示得出的下列结论中不正确的是( )
分别表示X、Y、Z三种不同的气体分子,其在一定条件下的变化如图所示,通过图示得出的下列结论中不正确的是( )
 已知
已知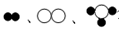 分别表示X、Y、Z三种不同的气体分子,其在一定条件下的变化如图所示,通过图示得出的下列结论中不正确的是( )
分别表示X、Y、Z三种不同的气体分子,其在一定条件下的变化如图所示,通过图示得出的下列结论中不正确的是( )| A. | 在化学变化中,分子一定发生变化 | B. | 该反应可表示为4X+Y═2Z | ||
| C. | 分子之间有间隔 | D. | 一个Z分子由四个原子构成 |