题目内容
把生锈的铁钉放入足量的稀盐酸中,刚开始出现的现象是 ,其反应的化学方程式是 ,一段时间后又有气泡放出其原因用化学方程式表示为 .
【考点】酸的化学性质;书写化学方程式、文字表达式、电离方程式.
【专题】常见的酸 酸的通性.
【分析】把生锈的铁钉放到足量的稀盐酸中,铁锈的主要成分为氧化铁,所以表面的铁锈先与盐酸反应,当铁锈反应完后,铁继续与盐酸反应;可以据此解答该题.
【解答】解:铁锈的主要成分是Fe2O3,它会与稀盐酸反应,生成的Fe3+显黄色,其反应的化学方程式为:Fe2O3 +6HCl═2FeCl3+3H2O,当铁锈反应完后,铁继续与盐酸反应,该反应的化学方程式为:Fe+2HCl═FeCl2+H2↑,所以会观察到有气泡冒出.
答案:铁锈溶解、生成黄色溶液; Fe2O3 +6HCl═2FeCl3+3H2O;Fe+2HCl═FeCl2+H2↑.
【点评】对于实验过程中出现的现象,同学们要会灵活应用化学知识去作答,明确在置换反应中,铁表现出正二价,正二价的金属铁溶液呈浅绿色,而三价铁溶液呈黄色.

 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表.则关于此反应的说法正确的是( )
| 物 质 | X | Y | Z | W |
| 反应前的质量(g) | 2 | 1 | 16 | 16 |
| 反应后的质量(g) | 12 | m | 8 | 14 |
A.物质Y一定是该反应的催化剂
B.该反应的基本类型为分解反应
C.参加反应的Z与W的质量比为4:1
D.反应后生成X的质量为12 g
 段时间后,质量明显减少的是( )
段时间后,质量明显减少的是( )  B.浓盐酸 C.氢氧化钠 D.氯化钠
B.浓盐酸 C.氢氧化钠 D.氯化钠

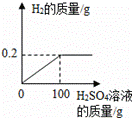 (1)18g该样品中锌的质量.
(1)18g该样品中锌的质量.