题目内容
19.在一定条件下,下列物质间的转化通过一步反应就能实现的是( )①甲烷→炭黑
②熟石灰→烧碱
③蛋白质→氨基酸
④铜→硝酸铜.
| A. | ②④ | B. | ①②④ | C. | ①②③ | D. | ①②③④ |
分析 可以根据物质的性质,结合具体的反应进行分析.
①甲烷→炭黑,隔绝空气加强热,能通过一步反应实现;
②熟石灰→烧碱,可以通过熟石灰和碳酸钠反应生成烧碱,一步就可完成;
③蛋白质→氨基酸能通过一步反应实现;
④铜→硝酸铜,铜和硝酸银反应会生成硝酸铜和银.
解答 解:①甲烷→炭黑,隔绝空气加强热,化学反应是:CH4$\frac{\underline{\;高温\;}}{\;}$C+2H2能通过一步反应实现;
②熟石灰→烧碱,可以通过熟石灰和碳酸钠反应生成烧碱和碳酸钙沉淀,一步就可完成;
③蛋白质→氨基酸,蛋白质在酶作用下可以转化为氨基酸,能通过一步反应实现;
④碳酸氢铵→氨气,铜→硝酸铜,铜和硝酸银反应会生成硝酸铜和银,能通过一步反应实现.
所以物质间的转化能通过一步反应实现的是:①②③④,故选:D.
点评 本题考查了常见物质间的转化,完成此题,可以依据物质的性质结合具体的反应进行.

练习册系列答案
相关题目
9.根据化学方程式2C2H2+XO2=4CO2+2H2O,推断X为( )
| A. | 2 | B. | 3 | C. | 5 | D. | 6 |
10.某同学用量筒量取一定体积的液体,量筒放平稳.先仰视液面,读数为16mL,倾倒部分液体后,又俯视液面,读数为10mL,则该同学实际倾倒的液体的体积为( )
| A. | 等于6mL | B. | 大于6mL | C. | 小于6mL | D. | 无法判断 |
7.卟啉铁(C34H32ClFeN4O4)对人体缺铁性贫血有显著疗效.以下说法正确的是( )
| A. | 卟啉铁中含有5种元素 | |
| B. | 1个卟啉铁分子中含有34个碳原子 | |
| C. | 卟啉铁中碳、氢元素的质量比为17:16 | |
| D. | “缺铁性贫血”中的“铁”指单质铁 |
4.广西高铁建设中,常用铝和氧化铁(Fe2O3)高温条件下,反应生成熔融状态下的铁单质对钢轨中的缝隙进行焊接.反应的化学方程式为:Fe2O3+2Al $\frac{\underline{\;高温\;}}{\;}$ X+2Fe,则X的化学式为( )
| A. | O2 | B. | H2O | C. | AlO | D. | Al2O3 |
8.化学是一门以实验为基础的学科,同学们在实验室进行了与氧气有关的一系列实验探究.
(一)探究空气中氧气的含量.甲设计了如下实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.(实验装置如图1所示)回答下列问题:
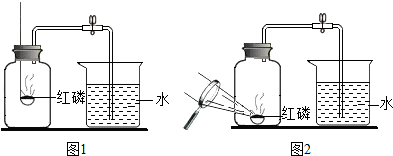
(1)实验过程中,观察到的主要现象是红磷燃烧,放出大量的热,生成大量白烟;烧杯中的水进入集气瓶约$\frac{1}{5}$处.反应的文字表达式是磷+氧气$\stackrel{点燃}{→}$五氧化二磷.
(2)乙用上述实验装置测定的结果是:空气中氧气含量与正常值有较明显的偏差,其操作上的原因可能是(要求答出两种):装置气密性不好,红磷量不足.
(3)丙也设计了一个实验方案,装置和操作同上,只不过用木炭代替了红磷.当木炭停止燃烧,集气瓶冷却至室温,打开铁夹后,水能否进入集气瓶?为什么?不会;碳与氧气反应生成了二氧化碳气体,没有产生压强差.
(4)某同学对实验进行反思后,提出改进方案(如图2所示),你认为改进后的优点是误差少或无污染.
(二)探究氧气的性质
(1)下列A、B两图是一同学进行的物质在氧气中燃烧的两个实验:

请帮助他完成实验报告,并回答有关问题.
B中反应的文字表达式为:硫+氧气$\stackrel{点燃}{→}$二氧化硫;该反应属于化合反应.两集气瓶中都预先装有少量水,但作用不同,A中水的作用是防止高温生成物溅落瓶底,引起集气瓶炸裂.
(2)图C是某同学为证明呼出的气体中二氧化碳比吸入的空气中含量高设计的实验,我认为不能(填“能”或“不能”)达到到实验目的,如果不能请说明改进措施还增加一个盛有空气的集气瓶作对比实验.(如果能则该问题不必回答)
(一)探究空气中氧气的含量.甲设计了如下实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.(实验装置如图1所示)回答下列问题:

(1)实验过程中,观察到的主要现象是红磷燃烧,放出大量的热,生成大量白烟;烧杯中的水进入集气瓶约$\frac{1}{5}$处.反应的文字表达式是磷+氧气$\stackrel{点燃}{→}$五氧化二磷.
(2)乙用上述实验装置测定的结果是:空气中氧气含量与正常值有较明显的偏差,其操作上的原因可能是(要求答出两种):装置气密性不好,红磷量不足.
(3)丙也设计了一个实验方案,装置和操作同上,只不过用木炭代替了红磷.当木炭停止燃烧,集气瓶冷却至室温,打开铁夹后,水能否进入集气瓶?为什么?不会;碳与氧气反应生成了二氧化碳气体,没有产生压强差.
(4)某同学对实验进行反思后,提出改进方案(如图2所示),你认为改进后的优点是误差少或无污染.
(二)探究氧气的性质
(1)下列A、B两图是一同学进行的物质在氧气中燃烧的两个实验:

请帮助他完成实验报告,并回答有关问题.
| 物质 | 现象 | |
| 在空气中 | 在氧气中 | |
| 铁丝 | 红热 | 剧烈燃烧,火星四射,放出大量的热,生成黑色固体 |
| 硫 | 微弱的淡蓝色火焰 | 明亮的蓝紫色火焰,放出大量的热,生成有刺激性气味的气体 |
(2)图C是某同学为证明呼出的气体中二氧化碳比吸入的空气中含量高设计的实验,我认为不能(填“能”或“不能”)达到到实验目的,如果不能请说明改进措施还增加一个盛有空气的集气瓶作对比实验.(如果能则该问题不必回答)
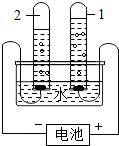 如图是电解水实验装置.
如图是电解水实验装置.