题目内容
5.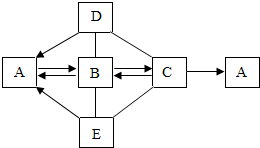 A-E是初中化学常见的五种物质,D、E是氧化物.常温下,B是气体,D是黑色固体,E是红棕色固体. A、B、C含氢元素,胃液中含C.短线“-”表示两种物质可以发生化学反应,箭头“→”表示一种物质能转化为另一种物质.请回答下列问题:
A-E是初中化学常见的五种物质,D、E是氧化物.常温下,B是气体,D是黑色固体,E是红棕色固体. A、B、C含氢元素,胃液中含C.短线“-”表示两种物质可以发生化学反应,箭头“→”表示一种物质能转化为另一种物质.请回答下列问题:(1)写出下列物质的化学式:AH2O、CHCl.
(2)B与D反应生成红色固体,该反应的化学方程式为CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$ Cu+H2O.
(3)C与E反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O.请写出该反应的一个用途除锈.
分析 根据题干提供的信息进行分析解答,根据“E是红棕色固体”,且是氧化物,故E是氧化铁;根据“D是黑色固体”,且是氧化物,故D可能是氧化铜;根据“常温下,B是气体”,且含有氢元素,故B是氢气,根据“胃液中含C”,且含有氢元素,则C为氯化氢;结合图框,推测A可能为水.据此解答.
解答 解:根据“E是红棕色固体”,且是氧化物,故E是氧化铁;根据“D是黑色固体”,且是氧化物,故D可能是氧化铜;根据“常温下,B是气体”,且含有氢元素,故B是氢气,根据“胃液中含C”,且含有氢元素,则C为氯化氢;结合图框,推测A可能为水.代入检验,符合题意.
(1)根据分析,可知A为水,C为氯化氢,其化学式分别为:H2O、HCl.
(2)根据分析,可知B与D反应,即氧化铜与氢气反应生成红色固体和水,该反应的化学方程式为CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$ Cu+H2O.
(3)根据分析,可知C与E反应,即氧化铁与稀盐酸反应,其化学方程式为Fe2O3+6HCl=2FeCl3+3H2O.该反应的一个用途除锈.
故答案为:
(1)H2O; HCl; (2)CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$ Cu+H2O;
(3)Fe2O3+6HCl=2FeCl3+3H2O; 除锈
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
相关题目
17.今年初,纪录片《穹顶之下》再次引起了社会对空气质量的热议.以下不属于空气污染物的是( )
| A. | CO2 | B. | SO2 | C. | 可吸入颗粒物 | D. | NO2 |
15.为了验证铁、锌、铜三种金属的活动性顺序,某同学设计了下列四种方案,其中一定能达到实验目的是( )
| A. | 将Zn、Cu分别加入到FeSO4溶液中 | |
| B. | 把Zn分别加入到CuSO4溶液、FeSO4溶液中 | |
| C. | 把Zn、Cu分别加入到ZnSO4溶液中 | |
| D. | 把Cu分别加入到FeSO4溶液、ZnSO4溶液中 |
 下列概念符合图关系的是( )
下列概念符合图关系的是( )