题目内容
8.实验室里现有氯酸钾、二氧化锰、稀硫酸、石灰石和稀盐酸,以及下列仪器: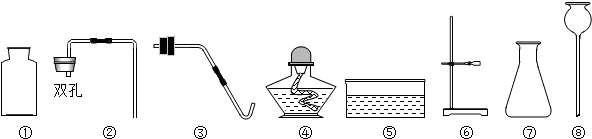
(1)利用上述仪器和药品可以制取二氧化碳,请你组装一套可以随时添加液体药品的制取装置,你选择的仪器是①②⑦⑧(填序号),药品是石灰石和稀盐酸;
(2)若补充一种仪器试管(填仪器名称),再利用上述仪器和药品还可以制取氧气,你选择的仪器是①③④⑤⑥(填序号);若用排水法收集,收集气体前,应将集气瓶装满水并盖上玻璃片;
(3)质量相同的下列四种物质,完全分解后制得氧气质量最多的是D.
A.H2O2 B.KMnO4 C.KClO3 D.H2O.
分析 根据气体发生装置的选择依据反应物的状态和反应的条件,根据化学方程式可以判断各种物质分解产生氧气的质量.
解答 解:(1)用石灰石和稀盐酸制取二氧化碳,是固体和液体在常温下的反应,选择的制取仪器有①②⑦⑧,药品为石灰石和稀盐酸;故填:①②⑦⑧;石灰石和稀盐酸;
(2)使用氯酸钾制取氧气,需要将氯酸钾放在试管中加热,需要的仪器有①③④⑤⑥,若用排水法收集,收集气体前,应将集气瓶装满水,并盖上玻璃片;
故填:试管;①③④⑤⑥;水;玻璃片;
(3)氯酸钾、高锰酸钾、过氧化氢、水分解的化学方程式分别是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑、2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑、2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$H2O+O2↑、
2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,由化学方程式可知,高锰酸钾中的氧元素一部分转化到锰酸钾和二氧化锰中,一部分转化成氧气,过氧化氢中的氧元素一部分转化到水中,一部分转化成氧气,而氯酸钾和水中的氧元素完全转化成氧气,因此完全分解后制得氧气质量最多的是氯酸钾和水中的一种,
设氯酸钾和水的质量都是x,
质量为x的氯酸钾中氧元素的质量为:x×$\frac{48}{122.5}$×100%=0.39x,
质量为x的水中氧元素的质量为:x×$\frac{16}{18}$×100%=0.89x,
由计算可知,下列四种物质,完全分解后制得氧气质量最多的是水.
故选:D.
点评 本题考查了常见气体的实验室制取,考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.完成此题,可以依据已有的知识进行.

| A. | 4:1 | B. | 5:1 | C. | 6:1 | D. | 7:1 |
| 成分 | 水 | 蛋白质 | 脂肪 | 糖类 | 钙 | 磷 | 铁 | 维生素A |
| 质量分数/% | 96.0 | 1.8 | 0.7 | 1.1 | 0.01 | 0.03 | 0.0005 | 0.015 |
(2)在豆浆所含的营养成分中糖类是供给人体能量最主要的营养素.