题目内容
4.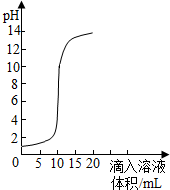 如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.
如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.(1)氢氧化钠和盐酸恰好完全反应时,溶液的pH=7(填“<”、“>”或“=”).
(2)当滴入溶液的体积为15mL时所得溶液中的溶质为NaCl、NaOH(写化学式),若在此溶液中滴入石蕊试液,溶液呈蓝色.
分析 (1)强酸强碱恰好中和时,溶液显中性;
(2)当溶液的pH<7时,溶液显酸性,当溶液的pH>7时,溶液显碱性,当溶液的pH=7时,溶液显中性;根据盐酸和氢氧化钠的反应原理以及图象数据来回答.
解答 解:(1)氢氧化钠和盐酸恰好完全反应时,氢离子和氢氧根离子均无剩余,溶液显中性,pH=7,故答案为:等于;
(2)盐酸和氢氧化钠的反应原理是:HCl+NaOH=NaCl+H2O,滴入氢氧化钠溶液的体积为15mL时,溶液仍为碱性,所以是氢氧化钠过量,所得溶液中的溶质有生成的氯化钠也有剩余的氢氧化钠,若在此溶液中滴入石蕊试液,溶液呈蓝色.
故答案为:(1)=;(2)NaCl、NaOH;蓝.
点评 酸碱中和反应结合图象知识来考查,难度较大,考查的知识面较广.

练习册系列答案
 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案
相关题目
14.下列各组物质能够在溶液中大量共存的是( )
| A. | KCl、NaNO3 | B. | HCl、NaHCO3 | C. | NaCl、AgNO3 | D. | H2SO4、NaOH |
15.在粗盐提纯的实验中,下列操作正确的是( )
| A. |  粗盐称量 | B. |  粗盐溶解 | C. |  浊液过滤 | D. |  蒸发结晶 |
19.日常生活中,区别下列各组物质的做法错误的是( )
| A. | 用肥皂水区分硬水和软水 | |
| B. | 用尝味道的方法区分厨房橱柜中调味品食盐和蔗糖 | |
| C. | 用灼烧的方法鉴别羊毛线和棉线 | |
| D. | 用白醋区分苏打和小苏打 |
9.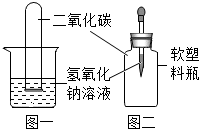 某学习小组的同学做实验,向盛有少量氢氧化钠溶液的试管中通入二氧化碳,未看到明显的实验现象.
某学习小组的同学做实验,向盛有少量氢氧化钠溶液的试管中通入二氧化碳,未看到明显的实验现象.
【提出问题】氢氧化钠能否与二氧化碳反应?
【猜想与假设】亮亮同学认为氢氧化钠能与二氧化碳反应;莉莉同学认为氢氧化钠不能与二氧化碳反应.
【设计与实验】亮亮同学设计了两个装置并进行实验.请你和他一起验证他的猜想.
【反思与评价】莉莉同学提出质疑,认为上述现象可能是二氧化碳溶于水的结果.
【设计与实验】请你设计一个实验,证明氢氧化钠确实与二氧化碳反应.
【交流与提高】实验证明氢氧化钠还能与二氧化硫反应,化学方程式为:2NaOH+SO2═X+H2O,X的化学式是Na2SO4.
 某学习小组的同学做实验,向盛有少量氢氧化钠溶液的试管中通入二氧化碳,未看到明显的实验现象.
某学习小组的同学做实验,向盛有少量氢氧化钠溶液的试管中通入二氧化碳,未看到明显的实验现象.【提出问题】氢氧化钠能否与二氧化碳反应?
【猜想与假设】亮亮同学认为氢氧化钠能与二氧化碳反应;莉莉同学认为氢氧化钠不能与二氧化碳反应.
【设计与实验】亮亮同学设计了两个装置并进行实验.请你和他一起验证他的猜想.
| 实验步骤 | 实验现象 | 实验结论 |
| 如图一,将收集满二氧化碳的试管倒置于氢氧化钠溶液中 | 试管内液面上升 | 二氧化碳和氢氧化钠发生了反应 |
| 如图二, | 塑料瓶变瘪 |
【设计与实验】请你设计一个实验,证明氢氧化钠确实与二氧化碳反应.
| 实验步骤 | 实验现象 | 实验结论 |
取少量塑料瓶中的液体于试管中,滴加稀盐酸 | 有气泡产生 | 氢氧化钠与二氧化碳反应 |
16. 现有甲、乙、丙三种金属,采用将其中的一种金属分别放入另外两种金属的硫酸盐溶液中的方法进行实验,得到三种金属间的转化关系(如图所示),则三种金属活动性由强到弱的顺序是( )
现有甲、乙、丙三种金属,采用将其中的一种金属分别放入另外两种金属的硫酸盐溶液中的方法进行实验,得到三种金属间的转化关系(如图所示),则三种金属活动性由强到弱的顺序是( )
 现有甲、乙、丙三种金属,采用将其中的一种金属分别放入另外两种金属的硫酸盐溶液中的方法进行实验,得到三种金属间的转化关系(如图所示),则三种金属活动性由强到弱的顺序是( )
现有甲、乙、丙三种金属,采用将其中的一种金属分别放入另外两种金属的硫酸盐溶液中的方法进行实验,得到三种金属间的转化关系(如图所示),则三种金属活动性由强到弱的顺序是( )| A. | 乙、甲、丙 | B. | 乙、丙、甲 | C. | 丙、甲、乙 | D. | 丙、乙、甲 |
13.研究和学习化学,有许多重要方法.下列方法中所举示例错误的是( )
| 选项 | 方法 | 示例 |
| A | 实验法 | 用磷做“测定空气中氧气含量”的实验 |
| B | 分类法 | 根据组成物质的元素种类,将纯净物分为单质和化合物 |
| C | 归纳法 | 根据稀盐酸、稀硫酸等物质的化学性质,归纳出酸的通性 |
| D | 类比法 | 根据金属铝能与稀盐酸反应,推测金属铜也能与稀盐酸反应 |
| A. | A | B. | B | C. | C | D. | D |
19.下列离子可在pH值为4的溶液中大量共存,形成无色溶液的是( )
| A. | H+、Na+、NO3-、SO42- | B. | Ba2+、NO3-、CO32-、K+ | ||
| C. | Ba2+、Cu2+、NO3-、SO42- | D. | Ag+、NO3-、Mg2+、Cl- |