题目内容
13.有一块由两种金属组成的合金,其质量是21g,投入足量稀硫酸中,充分反应后收集到1g氢气,合金可能是( )| A. | 铁和锌 | B. | 铁和镁 | C. | 铁和铜 | D. | 铁和铝 |
分析 铁和稀硫酸反应生成硫酸亚铁和氢气,锌和稀硫酸反应生成硫酸锌和氢气,镁和稀硫酸反应生成硫酸镁和氢气,铜不能和稀硫酸反应,铝和稀硫酸反应生成硫酸铝和氢气,根据反应的化学方程式及其提供的数据可以进行相关方面的计算和判断.
解答 解:A、铁、锌和稀硫酸反应的化学方程式及其质量关系为:
Fe+H2SO4=FeSO4+H2↑,Zn+H2SO4═ZnSO4+H2↑,
56 2 65 2
由以上质量关系可知,反应生成1g氢气时需要单独消耗28g铁,单独消耗32.5g锌,当铁和锌的合金质量是21g时,与稀硫酸反应生成氢气的质量小于1g,该选项组成不可能;
B、铁、镁和稀硫酸反应的化学方程式及其质量关系为:
Fe+H2SO4=FeSO4+H2↑,Mg+H2SO4═MgSO4+H2↑,
56 2 24 2
由以上质量关系可知,反应生成1g氢气时需要单独消耗28g铁,单独消耗12g镁,当铁和镁的合金质量是21g时,与稀硫酸反应生成氢气的质量可能是1g,该选项组成可能;
C、铜不能和稀硫酸反应,铁和稀硫酸反应的化学方程式及其质量关系为:
Fe+H2SO4=FeSO4+H2↑,
56 2
由以上质量关系可知,反应生成1g氢气时需要单独消耗28g铁,即使21g都是铁,生成氢气的质量小于1g,该选项组成不可能;
D、铁、铝和稀硫酸反应的化学方程式及其质量关系为:
Fe+H2SO4=FeSO4+H2↑,2Al+3H2SO4═Al2(SO4)3+3H2↑
56 2 54 6
由以上质量关系可知,反应生成1g氢气时需要单独消耗28g铁,单独消耗9g铝,当铁和铝的合金质量是21g时,与稀硫酸反应生成氢气的质量可能是1g,该选项组成可能.
故选:BD.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

| A. | 溶液:溶质=4:1 | B. | 溶液:溶质=5:1 | C. | 溶剂:溶质=4:1 | D. | 溶剂:溶质=5:1 |
| A. | 蜡烛在空气中燃烧时产生明亮的火焰,同时放出较多热量 | |
| B. | 蜡烛燃烧时冒出的黑烟与吹灭蜡烛时产生的白烟是同种物质 | |
| C. | 蜡烛燃烧的生成物主要是水和二氧化碳 | |
| D. | 蜡烛燃烧属于化学变化,其过程中同时有物理变化发生 |
 ”、“
”、“ ”表示不同种元素的原子.
”表示不同种元素的原子.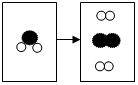
 B、
B、 C、
C、
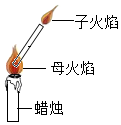 1860年,英国化学家法拉第在为少年儿童所做的化学讲座中用蜡烛和玻璃导管做了一个十分有趣的“子母火焰”实验,如图.
1860年,英国化学家法拉第在为少年儿童所做的化学讲座中用蜡烛和玻璃导管做了一个十分有趣的“子母火焰”实验,如图.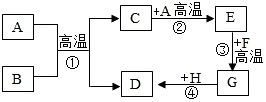 A~H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,它们的转化关系如图所示.请回答:
A~H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,它们的转化关系如图所示.请回答: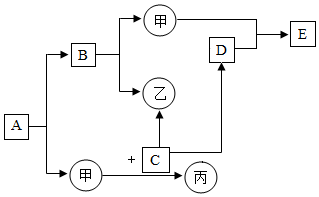 如图中A、B、C、D、E、甲、乙、丙均为初中化学中常见物质,其中B在常温下为最常见液体,A也是液体且和B的元素组成相同,甲、乙为常见气体,D为红色金属单质,C为常见的银白色金属单质、E、丙都为黑色固体,其余反应条件、部分反应物和生成物均已略去.试推断并回答有关问题:
如图中A、B、C、D、E、甲、乙、丙均为初中化学中常见物质,其中B在常温下为最常见液体,A也是液体且和B的元素组成相同,甲、乙为常见气体,D为红色金属单质,C为常见的银白色金属单质、E、丙都为黑色固体,其余反应条件、部分反应物和生成物均已略去.试推断并回答有关问题: