题目内容
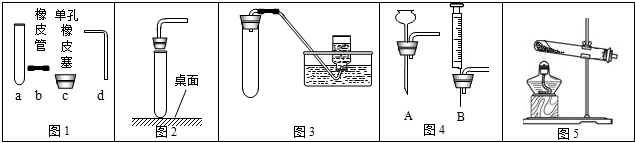
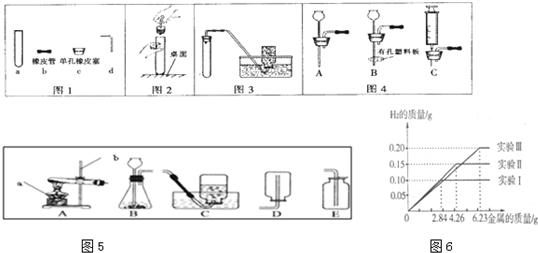
化学是一门以实验为基础的学科,化学所取得的丰硕成果,是与实验的重要作用分不开的.结合下列实验装置图回答问题:

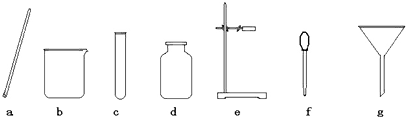
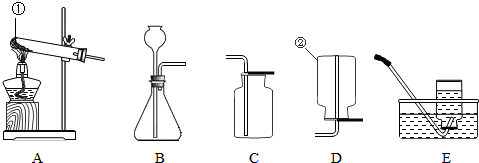
(1)写出指定仪器的名称:①
(2)写出实验室中用高锰酸钾制取氧气的化学方程式:
(3)实验室收集氧气时,可选用的收集装置是
(4)实验室制取二氧化碳时,可选用的发生装置是
(5)收集二氧化碳时可以选择装置D,理由是

(1)写出指定仪器的名称:①
分液漏斗
分液漏斗
;②集气瓶
集气瓶
.(2)写出实验室中用高锰酸钾制取氧气的化学方程式:
2KMnO4
K2MnO4+MnO2+O2↑
| ||
2KMnO4
K2MnO4+MnO2+O2↑
.
| ||
(3)实验室收集氧气时,可选用的收集装置是
D或E
D或E
(填字母代号).(4)实验室制取二氧化碳时,可选用的发生装置是
B
B
(填字母代号),写出化学反应方程式CaCO3+2HCl═CaCl2+CO2↑+H2O
CaCO3+2HCl═CaCl2+CO2↑+H2O
.(5)收集二氧化碳时可以选择装置D,理由是
二氧化碳密度比空气大且不与氧气反应
二氧化碳密度比空气大且不与氧气反应
,也可以选择装置E,理由是因为CO2溶解性有限,从导管口产生的气泡在水中能较快浮起而逸出
因为CO2溶解性有限,从导管口产生的气泡在水中能较快浮起而逸出
.分析:(1)熟记常见仪器的名称和作用;
(2)根据高锰酸钾加热生成锰酸钾、二氧化锰和氧气进行解答;
(3)根据氧气的性质来选择收集装置;
(4)实验室是用碳酸钙和稀盐酸反应制取二氧化碳,条件不需要加热来选用发生装置;
(5)根据二氧化碳的性质来选择收集装置.
(2)根据高锰酸钾加热生成锰酸钾、二氧化锰和氧气进行解答;
(3)根据氧气的性质来选择收集装置;
(4)实验室是用碳酸钙和稀盐酸反应制取二氧化碳,条件不需要加热来选用发生装置;
(5)根据二氧化碳的性质来选择收集装置.
解答:解:(1)熟记常见仪器的名称:①分液漏斗;②集气瓶;
(2)高锰酸钾加热生成锰酸钾、二氧化锰和氧气,反应的化学方程式:2KMnO4
K2MnO4+MnO2+O2↑;
(3)氧气的密度大于空气的密度,可用向上排空气法收集;氧气不易溶于水,可用排水法收集;
(4)实验室是用碳酸钙和稀盐酸反应制取二氧化碳且条件不需要加热,所以收集装置可用B装置;反应的化学反应方程式:CaCO3+2HCl═CaCl2+CO2↑+H2O;
(5)二氧化碳的密度大于空气的密度,收集二氧化碳时可以选择装置D;因为CO2溶解性有限,从导管口产生的气泡在水中能较快浮起而逸出,所以也可以选择装置E.
故答案为:(1)①分液漏斗;②集气瓶;
(2)2KMnO4
K2MnO4+MnO2+O2↑;
(3)D或E;
(4)B;CaCO3+2HCl═CaCl2+CO2↑+H2O;
(5)二氧化碳密度比空气大且不与氧气反应;因为CO2溶解性有限,从导管口产生的气泡在水中能较快浮起而逸出.
(2)高锰酸钾加热生成锰酸钾、二氧化锰和氧气,反应的化学方程式:2KMnO4
| ||
(3)氧气的密度大于空气的密度,可用向上排空气法收集;氧气不易溶于水,可用排水法收集;
(4)实验室是用碳酸钙和稀盐酸反应制取二氧化碳且条件不需要加热,所以收集装置可用B装置;反应的化学反应方程式:CaCO3+2HCl═CaCl2+CO2↑+H2O;
(5)二氧化碳的密度大于空气的密度,收集二氧化碳时可以选择装置D;因为CO2溶解性有限,从导管口产生的气泡在水中能较快浮起而逸出,所以也可以选择装置E.
故答案为:(1)①分液漏斗;②集气瓶;
(2)2KMnO4
| ||
(3)D或E;
(4)B;CaCO3+2HCl═CaCl2+CO2↑+H2O;
(5)二氧化碳密度比空气大且不与氧气反应;因为CO2溶解性有限,从导管口产生的气泡在水中能较快浮起而逸出.
点评:此题考查的是气体的制取原理和装置的选择.只要掌握气体的制取原理,掌握装置选择的依据,问题就能迎刃而解.

练习册系列答案
相关题目
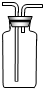
 20、化学是一门以实验为基础的科学,规范的实验操作是实验成功的前提,请回答:
20、化学是一门以实验为基础的科学,规范的实验操作是实验成功的前提,请回答: