题目内容
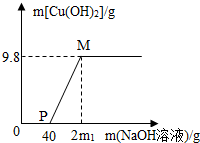 向含有CuCl2和HCl的混合溶液100g中,逐滴加入10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图,仅考虑沉淀为Cu(OH)2.
向含有CuCl2和HCl的混合溶液100g中,逐滴加入10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图,仅考虑沉淀为Cu(OH)2.(1)M点溶液中的溶质有
(2)计算P点溶液中氯化钠的质量分数,写出必要的计算过程.(结果精确到0.1%)
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据向含有CuCl2和HCl的混合溶液中,逐滴加入的NaOH溶液,氢氧化钠溶液先与盐酸反应生成氯化钠和水,所以开始没有沉淀生成,当盐酸反应后氢氧化钠溶液和氯化铜反应生成氢氧化铜沉淀和氯化钠,所以M点是氢氧化钠溶液和氯化铜溶液恰好反应,溶液中的溶质只有氯化钠进行解答;
(2)根据P点是氢氧化钠溶液恰好盐酸反应生成氯化钠和水,消耗氢氧化钠溶液的质量为40g,利用氢氧化钠的质量求出生成氯化钠的质量,进而求出溶液中氯化钠的质量分数即可.
(2)根据P点是氢氧化钠溶液恰好盐酸反应生成氯化钠和水,消耗氢氧化钠溶液的质量为40g,利用氢氧化钠的质量求出生成氯化钠的质量,进而求出溶液中氯化钠的质量分数即可.
解答:解:(1)向含有CuCl2和HCl的混合溶液中,逐滴加入的NaOH溶液,氢氧化钠溶液先与盐酸反应生成氯化钠和水,所以开始没有沉淀生成,当盐酸反应后氢氧化钠溶液和氯化铜反应生成氢氧化铜沉淀和氯化钠,所以M点是氢氧化钠溶液和氯化铜溶液恰好反应,溶液中的溶质只有氯化钠一种;故填:1;
(2)设出生成氯化钠的质量为x.
NaOH+HCl═NaCl+H2O
40 58.5
40g×10% x
=
解得:x=5.85g
P点溶液中氯化钠的质量分数=
×100%=4.2%
答:P点溶液中氯化钠的质量分数为4.2%.
(2)设出生成氯化钠的质量为x.
NaOH+HCl═NaCl+H2O
40 58.5
40g×10% x
| 40 |
| 40g×10% |
| 58.5 |
| x |
解得:x=5.85g
P点溶液中氯化钠的质量分数=
| 5.85g |
| 100g+40g |
答:P点溶液中氯化钠的质量分数为4.2%.
点评:本题考查化学方程式与溶液的综合计算,解题关键是分析清楚反应过程的先后,找出每个过程中已知物质的质量.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
空气中含量较多,且能够用以填充食品包装袋的气体是( )
| A、氧气 | B、氮气 |
| C、稀有气体 | D、二氧化碳 |
已知:同温同压下,相同体积的任何气体所含分子数目相同.现将同温同压下的2L CO2和1L C2H2(乙炔)混合,所得混合气体中CO2和C2H2的分子数比是 ;混合气体中C、H、O三种元素的质量比是 .
推理是化学学习中常用的思维方法,下列推理正确的是( )
| A、制备氢氧化钠溶液:将饱和的Na2CO3溶液与过量的石灰水混合后过滤 |
| B、氧化物一定含氧元素,含氧元素的物质一定是氧化物 |
| C、中和反应生成盐和水,生成盐和水的反应一定是中和反应 |
| D、碱性较强的溶液能使酚酞溶液变红,能使酚酞溶液变红的溶液一定呈碱性 |
 纯碱样品中含有少量的氯化钠,某同学为测定纯碱样品中碳酸钠的含量,他取该纯碱样品12g,全部溶解在100g水中,再加入氯化钙溶液,所加氯化钙的质量如图所示.请计算:
纯碱样品中含有少量的氯化钠,某同学为测定纯碱样品中碳酸钠的含量,他取该纯碱样品12g,全部溶解在100g水中,再加入氯化钙溶液,所加氯化钙的质量如图所示.请计算: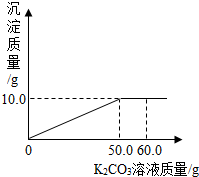 取KCl和CaCl2混合物15克,加入35克水完全溶解后,逐滴加入溶质质量分数为27.6%的K2CO3溶液,所加K2CO3溶液的质量的质量与生成沉淀质量的关系如图所示:
取KCl和CaCl2混合物15克,加入35克水完全溶解后,逐滴加入溶质质量分数为27.6%的K2CO3溶液,所加K2CO3溶液的质量的质量与生成沉淀质量的关系如图所示: