题目内容
15.请结合如图所示实验装置回答有关问题: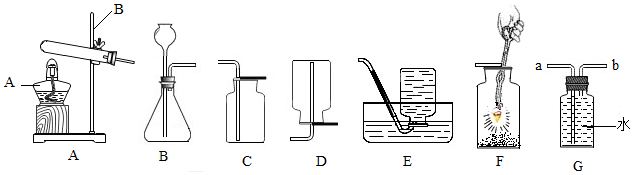
(1)书写实验仪器名称:A酒精灯,B铁架台.
(2)用过氧化氢溶液和二氧化锰来制取氧气时,该反应的文字表达式是过氧化氢$\stackrel{二氧化锰}{→}$水+氧气可选用的发生装置是B(填序号),其中二氧化锰起催化作用.
(3)高锰酸钾制取氧气时,写出反应的文字表达式高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气,根据该反应原理,可选择图中A(填标号)为发生装置.A装置试管口要略向下倾斜的原因是防止冷凝水回流,炸裂试管;试管口塞一团棉花的目的是防止高锰酸钾粉末进入导管.
(4)用装置C收集氧气,是因为氧气的性质是氧气的密度比空气大,此方法收集氧气的验满方法是把带火星的木条放在集气瓶口,木条复燃,证明集满.
(5)用E装置收集氧气,是因为氧气的性质是氧气不易溶于水,此方法收集氧气的验满方法是集气瓶口有气泡冒出,证明氧气集满.
(6)按图F作细铁丝在氧气中燃烧的实验,观察到的现象有铁丝剧烈燃烧,放热,生成黑色固体.写出发生反应的文字表达式是铁+氧气$\stackrel{点燃}{→}$四氧化三铁.实验过程中为了防止集气瓶底部破裂,需要采取的措施是在集气瓶底部放少量的水或细沙.
(7)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂.你认为上图中适合制取乙炔气体的发生装置是B,但是需要将其中的换成;如果用如图G所示装置收集乙炔,气体应从b(填“a”或“b”)端管口通入.
分析 (1)熟记仪器的名称;
(2)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
(3)根据高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,该反应的反应物是固体,反应条件需要加热,试管口要略向下倾斜的原因是防止冷凝水回流,炸裂试管;试管口塞一团棉花的目的是防止高锰酸钾粉末进入导管进行分析;
(4)根据氧气的密度比空气大,可以用向上排空气法收集进行分析;
(5)氧气不易溶于水,可以用排水法收集,所以收集氧气验满的方法是:集气瓶口有气泡冒出,证明氧气集满;
(6)根据铁和氧气在点燃的条件下生成四氧化三铁,以及注意事项进行分析;
(7)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须严格控制加水速度,以免剧烈反应加热引起发生装置炸裂.能控制反应速率的为B装置;乙炔微溶于水且密度比空气的小,可选择收集装置.
解答 解:(1)A是酒精灯,B是铁架台;故填:酒精灯;铁架台;
(2)用过氧化氢溶液和二氧化锰来制取氧气,为固液常温反应,发生装置选择B;反应的文字表达式为:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;其中二氧化锰在此化学反应中起催化作用.故填:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;B;催化;
(3)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,该反应的反应物是固体,反应条件需要加热,所以可选择图中A为发生装置;试管口要略向下倾斜的原因是防止冷凝水回流,炸裂试管;试管口塞一团棉花的目的是防止高锰酸钾粉末进入导管;故填:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;A;防止冷凝水回流,炸裂试管;防止高锰酸钾粉末进入导管;
(4)氧气的密度比空气大,可以用向上排空气法收集,所以收集氧气的验满方法是:把带火星的木条放在集气瓶口,木条复燃,证明集满;故填:氧气的密度比空气大;把带火星的木条放在集气瓶口,木条复燃,证明集满;
(5)氧气不易溶于水,可以用排水法收集,所以收集氧气验满的方法是:集气瓶口有气泡冒出,证明氧气集满;故填:氧气不易溶于水;集气瓶口有气泡冒出,证明氧气集满;
(6)铁和氧气在点燃的条件下生成四氧化三铁,实验过程中为了防止集气瓶底部破裂,需要采取的措施是:在集气瓶底部放少量的水或细沙.故填:铁+氧气$\stackrel{点燃}{→}$四氧化三铁;在集气瓶底部放少量的水或细沙;
(7)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须严格控制加水速度,以免剧烈反应加热引起发生装置炸裂.能控制反应速率的为B装置;乙炔微溶于水且密度比空气的小,如果用图所示装置收集乙炔,气体应从b端管口通入.故答案为:B;b.
点评 本题考查实验装置的选取,化学方程式的书写,考查知识点较多,但难度不大,只要对课本中的基础知识掌握了,就能做好此题.

| A. |  | B. |  | C. |  | D. |  |
| A. | 沉淀 | B. | 过滤 | C. | 吸附 | D. | 蒸馏 |
| A. | 氧化钙中含有少量碳酸钙可以通过高温煅烧的方法除去碳酸钙 | |
| B. | 鉴别CO和CO2两种无色气体,可观察它们哪个有毒,哪个无毒 | |
| C. | 鉴别蒸馏水和酒精两种无色液体,可以通过闻气味加以区别 | |
| D. | 除去CO2气体中混有的少量CO气体,可以使混合气体通过灼热的氧化铜 |
| A. | KCl溶液 | B. | 石蕊溶液 | C. | NaNO3溶液 | D. | 稀盐酸 |
(1)写出该中和反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O.
(2)探究烧杯内溶液中溶质的成分:
【作出猜想】
(A)溶质可能是CaCl2与Ca(OH)2
(B)溶质可能是CaCl2
(C)溶质可能是CaCl2与HCl
【查阅资料】CaCl2溶液呈中性
【实验设计】
①取少量烧杯中的溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.于是排除了猜想(A),你认为排除猜想(A)的理由是酚酞溶液不变色,说明溶液不呈碱性,而猜想A的溶液呈碱性,所以可以排除.
②小华想用碳酸钠溶液来验证后两种猜想,请你帮他完成实验,填写以下表格:
| 实验步骤 | 预计现象 | 预计结论 |
| 取少量反应后的溶液于试管中,逐滴加入碳酸钠溶液至过量 | 生成白色沉淀 | 猜想(B)正确 |
| 先有气泡产生,后产生白色沉淀 | 猜想(C)正确 |
A.取反应后的溶液于试管中,滴加紫色石蕊试液变红色
B.取反应后的溶液于试管中,加入锌粉冒气泡
C.用洁净的玻璃棒蘸取反应后的溶液,涂抹在pH试纸上,测溶液的pH<7
D.取反应后的溶液于试管中,加入硝酸银溶液,生成白色沉淀.


