题目内容
15.向一定质量的氢氧化钠溶液中加入50g溶质质量分数为9.8%的稀硫酸,恰好完全反应,所得溶液质量为75g.请计算:(1)50g稀硫酸中溶质的质量为4.9g.
(2)所用氢氧化钠溶液的溶质质量分数(写出计算过程).
分析 (1)根据溶质质量=溶液质量×溶质质量分数解答;
(2)根据质量守恒定律可知,参加反应的氢氧化钠溶液的质量为75g-50g=25g,根据氢氧化钠与硫酸反应的方程式,由稀硫酸中溶质的质量可求出氢氧化钠溶液中溶质的质量,再根据溶质质量分数的计算公式计算即可.
解答 解:
(1)50g稀硫酸中溶质的质量=50g×9.8%=4.9g
(2)由质量守恒定律可知,参加反应的氢氧化钠溶液的质量为75g-50g=25g,
设氢氧化钠溶液中溶质的质量x
H2SO4 +2NaOH=2H2O+Na2SO4
98 80
4.9g x
$\frac{98}{4.9g}$=$\frac{80}{x}$
x=4g
所用氢氧化钠溶液的溶质质量分数=$\frac{4g}{25g}$×100%=16%
答案:
(1)50g稀硫酸中溶质的质量为4.9g;
(2)所用氢氧化钠溶液的溶质质量分数为16%.
点评 本题主要考查学生运用化学方程式进行计算的能力,掌握相关的溶液及化学方程式基本计算是解题的关键所在.

练习册系列答案
相关题目
5.下图是实验室制取某些常见气体的装置图.根据所学知识回答:
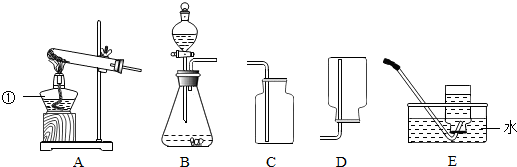
(1)写出仪器①的名称酒精灯;
(2)实验室用块状碳酸钙和稀盐酸制取二氧化碳,可选用B作为发生装置,选用C作为收
集装置.
(3)为了确定碳酸钙和稀盐酸反应后溶液的成分,小黄同学取用一定量的该溶液,向其中逐渐加入
一定质量分数的碳酸钠溶液,得到沉淀的质量与所加碳酸钠溶液的质量关系如下表所示:
分析数据可知:碳酸钙和稀盐酸反应后的溶液中的溶质是CaCl2(氯化钙)和HCl;表格中X为4克;
计算所加碳酸钠溶液的溶质质量分数?(写出计算过程)

(1)写出仪器①的名称酒精灯;
(2)实验室用块状碳酸钙和稀盐酸制取二氧化碳,可选用B作为发生装置,选用C作为收
集装置.
(3)为了确定碳酸钙和稀盐酸反应后溶液的成分,小黄同学取用一定量的该溶液,向其中逐渐加入
一定质量分数的碳酸钠溶液,得到沉淀的质量与所加碳酸钠溶液的质量关系如下表所示:
| 加入Na2CO3溶液的质量/克 | 20 | 40 | 60 | 80 | 100 |
| 生成沉淀的质量/克 | 0 | 1 | 3 | 4 | X |
计算所加碳酸钠溶液的溶质质量分数?(写出计算过程)
3.物质的性质决定其用途,下列说法错误的是( )
| A. | 石墨具有导电性,常用作电极 | |
| B. | 氧化钙能与水反应,可用作干燥剂 | |
| C. | 小苏打能与酸反应,可用于治疗胃酸过多 | |
| D. | 氢氧化钠溶液显碱性,常用于改良酸性土壤 |
 根据如图中标签上信息填空:
根据如图中标签上信息填空: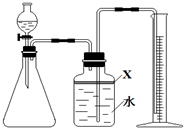 氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域.某氮化铝中含有碳或氧化铝杂质,某化学研究性学习小组设计并完成了如下实验.
氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域.某氮化铝中含有碳或氧化铝杂质,某化学研究性学习小组设计并完成了如下实验.