题目内容
9.生活处处有化学,下列说法正确的是( )| A. | 用甲醛浸泡海产品 | |
| B. | 用含小苏打的发酵粉烘制糕点 | |
| C. | 腌制的泡菜虽然含亚硝酸盐,但多吃无妨 | |
| D. | 用霉变的花生榨油 |
分析 A.根据甲醛有毒来分析;
B.根据小苏打的性质与用途来分析;
C.根据亚硝酸钠的毒性来分析;
D.根据霉变的花生中含有黄曲霉毒素来分析.
解答 解:A.甲醛是一种有毒物质,能致癌,所以不能用来浸泡海产品,故错误;
B.小苏打受热能分解产生二氧化碳,也可以和面粉发酵过程中产生的酸发生反应,生成大量的气体,从而使糕点变得松软和香甜;故正确;
C.亚硝酸钠是一种致癌物,过量食用会危害人体健康,故错误;
D.霉变的花生中含有黄曲霉毒素,黄曲霉毒素是一种致癌物,所以不能用霉变的花生榨油,故错误.
故选B.
点评 化学与生活生产有着紧密联系,学会用所学的化学知识,解决生活中的实际问题.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2. 分类、类比是学习化学常用的方法.请回答:
分类、类比是学习化学常用的方法.请回答:
(1)化学实验可按其主要目的分为:探究物质的性质、探究物质的含量、物质的制取等.据此应将下列实验中的A与D(填“B”或“C”或“D”)归为一类,依据是都属于物质的制取.
(2)以物质的类别为横坐标,物质中某元素的化合价为纵坐标所绘制的图象叫价类图,如图为硫的价类图,请分析该图后填空:
①A点表示的物质类别是纯净物中的单质;
②类比二氧化碳和水的反应,写出E点所对应的物质与水发生反应,生成F点所对应物质的化学方程式SO2+H2O═H2SO3.
 分类、类比是学习化学常用的方法.请回答:
分类、类比是学习化学常用的方法.请回答:(1)化学实验可按其主要目的分为:探究物质的性质、探究物质的含量、物质的制取等.据此应将下列实验中的A与D(填“B”或“C”或“D”)归为一类,依据是都属于物质的制取.
 |  |  |  |
| A | B | C | D |
①A点表示的物质类别是纯净物中的单质;
②类比二氧化碳和水的反应,写出E点所对应的物质与水发生反应,生成F点所对应物质的化学方程式SO2+H2O═H2SO3.
4. “侯氏制碱法”的生产原理是:先将氨气通入饱和食盐水中,再将压缩的二氧化碳通入饱和的氨盐水,得到碳酸氢钠晶体,分离得到的碳酸氢钠晶体充分受热分解后即可制得纯碱.
“侯氏制碱法”的生产原理是:先将氨气通入饱和食盐水中,再将压缩的二氧化碳通入饱和的氨盐水,得到碳酸氢钠晶体,分离得到的碳酸氢钠晶体充分受热分解后即可制得纯碱.
NaCl和NH4Cl的溶解度表:
请根据提供的信息,回答问题:
①10℃时,NaCl的溶解度是35.8g;
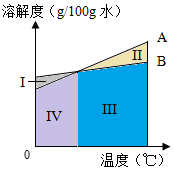
②图中,表示NH4Cl的溶解度曲线是A(填“A”或“B”)
③常温20℃时,配制的饱和食盐水的质量分数为26.5%,将食盐水的温度提高,溶液中溶质的质量分数也将提高,而实际生产中往往在常温下进行,这样做的理由是温度升高食盐的溶解度升高不多,因此质量分数也提高不多,而耗能大;
④若NaCl和NH4Cl溶液溶质质量分数相同,表示其溶液状态的点在图中可能位于的区域是I、II、III、IV(选填 I、II、III、IV);
⑤生产中通入氨气及二氧化碳,若要提高这些气体的溶解度,下列做法可行的是A(选填编号)
A.增大压强 B.升高温度 C.增加水量.
 “侯氏制碱法”的生产原理是:先将氨气通入饱和食盐水中,再将压缩的二氧化碳通入饱和的氨盐水,得到碳酸氢钠晶体,分离得到的碳酸氢钠晶体充分受热分解后即可制得纯碱.
“侯氏制碱法”的生产原理是:先将氨气通入饱和食盐水中,再将压缩的二氧化碳通入饱和的氨盐水,得到碳酸氢钠晶体,分离得到的碳酸氢钠晶体充分受热分解后即可制得纯碱.NaCl和NH4Cl的溶解度表:
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | |
| 溶解度 (g/100g水) | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | |
①10℃时,NaCl的溶解度是35.8g;
②图中,表示NH4Cl的溶解度曲线是A(填“A”或“B”)
③常温20℃时,配制的饱和食盐水的质量分数为26.5%,将食盐水的温度提高,溶液中溶质的质量分数也将提高,而实际生产中往往在常温下进行,这样做的理由是温度升高食盐的溶解度升高不多,因此质量分数也提高不多,而耗能大;
④若NaCl和NH4Cl溶液溶质质量分数相同,表示其溶液状态的点在图中可能位于的区域是I、II、III、IV(选填 I、II、III、IV);
⑤生产中通入氨气及二氧化碳,若要提高这些气体的溶解度,下列做法可行的是A(选填编号)
A.增大压强 B.升高温度 C.增加水量.
14.下列各组固体物质,只用水不能进行鉴别的是( )
| A. | CaCO3、Na2CO3 | B. | MnO2 CuO | C. | 生石灰、熟石灰 | D. | CuSO4、Fe2(SO4)3 |
1.化学方程式书写正确的是( )
| A. | CO+CuO$\stackrel{△}{→}$Cu+CO2↑ | B. | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 | ||
| C. | CaCO3→CaO+CO2↑ | D. | CO+O2 $\stackrel{点燃}{→}$ CO2 |