题目内容
12.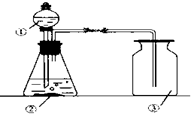 如图是实验室制取二氧化碳的装置图,
如图是实验室制取二氧化碳的装置图,(1)请填上编号的实验器材的名称:①分液漏斗
(2)该反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O
(3)集气瓶如此放置的理由是二氧化碳密度比空气大
(4)检验二氧化碳是否收集满的方法是将燃着的木条放在集气瓶口,木条熄灭,证明集满.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;
(3)根据二氧化碳的密度比空气大,可以采用向上排空气法收集进行分析;
(4)根据二氧化碳不具有助燃性进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,①是分液漏斗;
(2)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O;
(3)二氧化碳的密度比空气大,可以采用向上排空气法收集;
(4)二氧化碳不具有助燃性,所以验满的方法是:将燃着的木条放在集气瓶口,木条熄灭,证明集满.
故答案为:(1)分液漏斗;
(2)CaCO3+2HCl=CaCl2+CO2↑+H2O;
(3)二氧化碳密度比空气大;
(4)将燃着的木条放在集气瓶口,木条熄灭,证明集满.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
19.已知a克某纯碱样品中含有少量氯化钠,小曹同学为测定样品中纯碱的质量分数,进行如下实验设计和分析,假设空气中CO2忽略不计,且每步都完全反应,其中合理的是( )
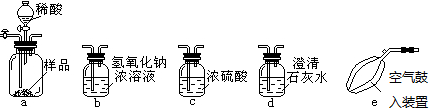

| A. | 选用30%的盐酸溶液与样品反应 | |
| B. | 按照e、a、b、c的顺序连接装置 | |
| C. | 本实验中只要测得装置b在实验前质量m1及实验后质量m2即可 | |
| D. | 根据所得数据,样品中纯碱质量分数为$\frac{{m}_{2}-{m}_{1}}{a}$×100% |
17.下列材料属于复合材料的是( )
| A. | 棉花 | B. | 陶瓷 | C. | 钢筋混凝土 | D. | 聚乙烯塑料 |
1.下列各组物质名称、化学符号、颜色完全一致的是( )
| A. | 液氧 O2 无色 | B. | 水 H2O2 无色 | ||
| C. | 二氧化锰 MnO2 黑色 | D. | 氯酸钾 KCl 白色 |
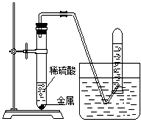 “化学反应条件的控制是实验的灵魂”.某校科学兴趣小组在老师指导下,进行了“比较金属活动性因素”的实验.请你帮助回答下列问题:
“化学反应条件的控制是实验的灵魂”.某校科学兴趣小组在老师指导下,进行了“比较金属活动性因素”的实验.请你帮助回答下列问题: 如图是甲、乙、丙三种固体的溶解度曲线,回答下列问题:
如图是甲、乙、丙三种固体的溶解度曲线,回答下列问题: