题目内容
有m克浓度为10%的NaCl溶液,若将其浓度增大到20%,可采用的方法是( )
A、蒸发掉溶剂质量的
| ||
B、蒸发掉
| ||
C、再溶解
| ||
D、再溶解
|
考点:有关溶质质量分数的简单计算
专题:溶液的组成及溶质质量分数的计算
分析:要使溶液的溶质质量分数变大,常通过两种方式:①加入溶质,②蒸发溶剂,据此结合溶质质量分数的计算进行分析判断.
解答:解:①若采取的是加入溶质的方法:设加入溶质的量是x,则有:mg×10%+x=(mg+x)×20%,解得x=
g.
②若采取的是蒸发溶剂的方法,设蒸发掉的溶剂是y,则有:mg×10%=(mg-y)×20%,解得y=
g.
A、采取蒸发溶剂的方法,应蒸发掉
g溶剂,本题中溶剂质量的一半小于
g,故选项采用的做法错误.
B、采取蒸发溶剂的方法,应蒸发掉
g溶剂,故选项采用的做法正确.
C、采取加入溶质的方法,应加入
g氯化钠固体,故选项采用的做法错误.
D、采取加入溶质的方法,应加入
g氯化钠固体,故选项采用的做法正确.
故选:BD.
| m |
| 8 |
②若采取的是蒸发溶剂的方法,设蒸发掉的溶剂是y,则有:mg×10%=(mg-y)×20%,解得y=
| m |
| 2 |
A、采取蒸发溶剂的方法,应蒸发掉
| m |
| 2 |
| m |
| 2 |
B、采取蒸发溶剂的方法,应蒸发掉
| m |
| 2 |
C、采取加入溶质的方法,应加入
| m |
| 8 |
D、采取加入溶质的方法,应加入
| m |
| 8 |
故选:BD.
点评:本题考查的是有关溶质质量分数的计算,分析出溶液的变化对溶液组成的影响、灵活运用溶质的质量分数的计算是正确解答此类题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列化学用语中,既能表示一种元素,又能表示一个原子,还能表示一种物质的是( )
| A、N2 |
| B、O |
| C、Fe |
| D、CO2 |
如图所示图象能正确反映相对应实验序号的是( )

①向pH为12的Ca(OH)2溶液中不断加水稀释
②向碳酸钙固体中逐滴加入稀盐酸至过量
③在40℃,将饱和的硝酸钾溶液恒温蒸发水分至有晶体析出
④将足量的金属镁片和锌片分别与等质量的相同质量分数的稀硫酸混合.

①向pH为12的Ca(OH)2溶液中不断加水稀释
②向碳酸钙固体中逐滴加入稀盐酸至过量
③在40℃,将饱和的硝酸钾溶液恒温蒸发水分至有晶体析出
④将足量的金属镁片和锌片分别与等质量的相同质量分数的稀硫酸混合.
| A、①② | B、③④ | C、②④ | D、①③ |
下列图象能正确反映对应变化关系的是
( )
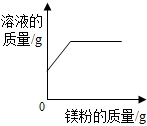 |  |  |  |
| A.向一定质量的稀盐酸中加入镁粉至过量 | B.用等质量、等溶质质量分数的双氧水分别制取氧气 | C.一定温度下,向不饱和硝酸钾溶液中加入硝酸钾 | D.等质量的镁粉和铁粉与足量相同溶质质量分数的盐酸反应 |
| A、A | B、B | C、C | D、D |
下列有关水的说法不正确的是( )
| A、过滤能除去天然水中所有的杂质 |
| B、生活中可以通过煮沸降低水的硬度 |
| C、城市浇花,使用喷灌、滴灌技术 |
| D、工业废水经过处理达标后再排放 |
 水是生命之源.请按要求回答下列问题:
水是生命之源.请按要求回答下列问题: 如图为氯化钠、碳酸钠在水中的溶解度曲线,请回答下列问题
如图为氯化钠、碳酸钠在水中的溶解度曲线,请回答下列问题