题目内容
对于反应X+3NaOH═3Y+Fe(OH)3↓,下列说法不正确的是( )
| A、X中含有三价元素 |
| B、X可能是FeCl3 |
| C、X可能是NaNO3 |
| D、Y中一定含有钠元素 |
考点:碱的化学性质,质量守恒定律及其应用
专题:常见的碱 碱的通性
分析:根据质量守恒定律中的元素种类不变和元素化合价在复分解反应中不变的特点,可得出本题答案.
解答:解:A、根据复分解反应特点,X中含有铁元素,又因为复分解反应中元素的化合价不变,所以X中含有三价的铁元素;
B、X中含有三价的铁元素,可能是FeCl3;
C、根据复分解反应特点,X中含有铁元素,不含钠元素;
D、根据复分解反应特点,Y中一定含有钠元素;
故选:C.
B、X中含有三价的铁元素,可能是FeCl3;
C、根据复分解反应特点,X中含有铁元素,不含钠元素;
D、根据复分解反应特点,Y中一定含有钠元素;
故选:C.
点评:本题主要考查质量守恒定律的应用和元素化合价在复分解反应中的特点,题目稍难.本题能加深学生对质量守恒定律中元素种类不变的认识,同时培养了学生的抽象思维能力.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
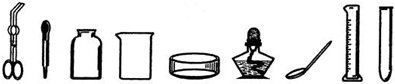
下列图示中,化学实验基本操作正确的是( )
A、 倾倒液体 |
B、 取粉末状固体药品 |
C、 过滤 |
D、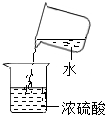 浓硫酸的稀释 |
如图所示的是实验室常用的实验装置.
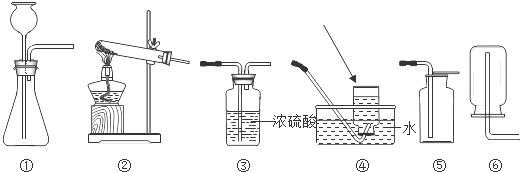
(1)图中示仪器中,箭头所示仪器名称为 和 .
(2)加热氯酸钾和二氧化锰固体制取氧气,反应中二氧化锰起 作用,其气体发生装置为 (填序号,下同),收集装置可以选取 .

(1)图中示仪器中,箭头所示仪器名称为
(2)加热氯酸钾和二氧化锰固体制取氧气,反应中二氧化锰起
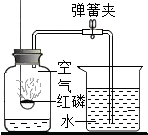 用如图装置测空气中氧气的含量,下列说法中不正确的是( )
用如图装置测空气中氧气的含量,下列说法中不正确的是( )| A、实验前一定要检验装置的气密性 | ||
| B、实验时红磷要过量 | ||
C、该实验证明空气中氧气的体积约占
| ||
| D、红磷燃烧产生大量的白烟,火焰熄灭后立刻打开弹簧夹 |
与金属跟盐反应的规律相似,非金属也有这样的规律.Br2、I2、Cl2及其化合物有如下关系
:Br2+2NaI=NaBr+I2 Cl2+2NaI=2NaCl+I2 Cl2+2NaBr═2NaCl+Br2,
则非金属单质Br2、I2、Cl2的化学活动性由强到弱的顺序为( )
:Br2+2NaI=NaBr+I2 Cl2+2NaI=2NaCl+I2 Cl2+2NaBr═2NaCl+Br2,
则非金属单质Br2、I2、Cl2的化学活动性由强到弱的顺序为( )
| A、Br2>I2>Cl2 |
| B、Br2>Cl2>I2 |
| C、Cl2>Br2>I2 |
| D、I2>Br2>Cl2 |
 为了测定一瓶过氧化氢溶液中溶质的质量分数,某同学取该溶液50g倒入烧杯中,然后向其中加入2g二氧化锰,烧杯内混合物的质量与反应时间的变化关系如图所示.
为了测定一瓶过氧化氢溶液中溶质的质量分数,某同学取该溶液50g倒入烧杯中,然后向其中加入2g二氧化锰,烧杯内混合物的质量与反应时间的变化关系如图所示.