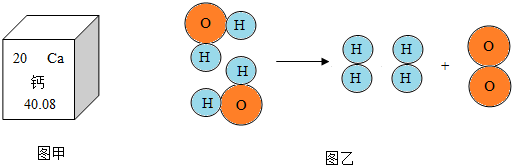
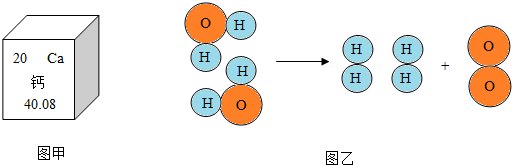
题目内容
如图是水分子分解示意图.下列叙述完全正确的是 ( )
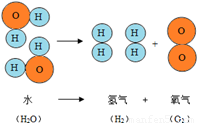
①水分解生成氢气和氧气;
②分子可以再分,原子不可以再分;
③物质都是由分子构成的;
④同种原子可以结合成分子,不同种原子不能结合成分子;
⑤同种物质的分子性质相同,不同种物质的分子性质不同。
A.①③ B.②④ C.①⑤ D.③④
C
【解析】
试题分析:①水分解生成氢气和氧气是正确的叙述;②分子可以再分,原子不可以再分是错误的叙述,因为原子不在化学变化中可以再分;③物质都是由分子构成的,是错误的叙述,因为构成物质的微粒由分子、原子、离子;④同种原子可以结合成分子,不同种原子不能结合成分子是错误的叙述,化合物的分子是由不同种原子结合成的;⑤同种物质的分子性质相同,不同种物质的分子性质不同。是正确的叙述,所以完全正确的叙述为 ①⑤,答案选择C
考点:分子的特征、水的电解

 阅读快车系列答案
阅读快车系列答案某化学兴趣小组利用“稀盐酸、硫酸铜、氢氧化钠、氯化钡”几种物质对复分
解反应进行再探究。
 【查阅资料】大多数强酸、强碱和盐类物质溶解于水时,在水
【查阅资料】大多数强酸、强碱和盐类物质溶解于水时,在水
分子的作用下发生了电离,产生了能够自由移动的阴、
阳离子。如图是HCl和NaOH在水中解离出离子的示意
图,HCl在水中会解离出H+和Cl-,NaOH在水中会解离
出Na+和OH-。以此类推,AgNO3在水中会解离出的离
子是 ▲ 和 ▲ (填离子符号)。
【提出问题】如何证明稀盐酸和氢氧化钠溶液发生反应了呢?
【实验设计】
| 实验步骤 | 实验现象 | 实验结论 |
| ▲ | ▲ | ▲ |
【反思质疑1】溶液中的离子都参加反应了吗?
【实验设计】
| 编号 | 实验 | 现象 |
| 1 | 向盛有CuSO4溶液的试管里加入适量的 NaCl溶液。 | 没有明显变化,溶液仍为蓝色 |
| 2 | 向盛有CuSO4溶液的试管里加入适量的 BaCl2溶液。 | 有 ▲ 生成,滤液为蓝色 |
【得出结论】通过对上述实验现象的分析,我们可以得出这样的结论:CuSO4溶液和
BaCl2溶液反应,实质参加反应的是Ba2+和SO42-,它们结合生成BaSO4沉淀,而
Cl-和Na+则是旁观者,并没有参加反应。
【反思质疑2】反应前后单位体积的溶液中能够自由移动的离子的数目有无改变?
 【研究讨论】稀盐酸与氢氧化钠溶液的反应我们可以用下图表示:
【研究讨论】稀盐酸与氢氧化钠溶液的反应我们可以用下图表示:
 |
 请你在下图圆圈中▲处将BaCl2溶液和CuSO4溶液反应的产物补充完整:
请你在下图圆圈中▲处将BaCl2溶液和CuSO4溶液反应的产物补充完整:
 |
【表达交流】通过上述探究我们可以得出酸碱盐在溶液中发生复分解反应的实质是: