题目内容
有一不纯的白色固体氯化镁中含有少量氯化钠。化学兴趣小组的同学为了测定该固体氯化镁中氯化钠的质量分数。进行了以下实验:称量10g样品置 于烧杯中,向其中加入90g水,搅拌,使其完全溶解为止。然后取该溶液一半,往其中滴加10%的氢氧化钠溶液,产生沉淀的质
于烧杯中,向其中加入90g水,搅拌,使其完全溶解为止。然后取该溶液一半,往其中滴加10%的氢氧化钠溶液,产生沉淀的质 量与所滴入氢氧化钠溶液的质量关系曲线如图所示。
量与所滴入氢氧化钠溶液的质量关系曲线如图所示。


试计算:(计算结果保留小数后1位)
(1)样品中氯化镁的质量;
(2)当滴入10%的氢氧化钠溶液至A点时,所得溶液中氯化钠的质量分数。
解:根据曲线图可得Mg(OH)2的质量==2.9 g (1分)
设MgCl2质量为X,参加反应的NaOH的质量为y,生成的NaCl的质量为Z。则:
MgCl2+2NaOH ==2NaCl+Mg(OH)2↓ (1分)
95 80 117 58
X Y×10% Z 2.9g
95:58= X:2.9g
X=95×2.9÷58
=4.75 g
样品中MgCl的质量:4 .75×2=9.5 g (1分)
.75×2=9.5 g (1分)
样品中NaCl的质量=(10-4.75×2)=0.5 g (1分)
80:58==Y×10%:2.9
Y=80×2.9÷5.8
=40g  (1分)
(1分)
117:58=Z:2.9g
Z=117×2.9÷58
=5.85 g (1分)
溶液中NaCl的总质量=5.85g +0.25g =6.1g (1分)
A点时,所得溶液中NaCl的质量分数=6.1g÷(50+40-2.9)×100%=7% (1分)
答:(略)
(注:其他解法只要合理,过程清楚,结果正确均应给分)

下表除杂质所选试剂正确的是 ( )
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | CaO | CaCO3 | 加入稀盐酸至不再产生气泡 |
| B | CO2气体 | HCl气体 | 通入NaOH溶液 |
| C | CO2气体 | CO气体 | 通过灼热的CuO |
| D | NaCl溶液 | Na2CO3 | 加入稀硫酸至不再产生 |


 滤
滤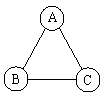 的关系如图所示(图中“ ”表示相连的两种物质能在溶液中发生
的关系如图所示(图中“ ”表示相连的两种物质能在溶液中发生 气泡
气泡