题目内容
7. 汽车是现代生活中不可缺少的工具之一.请回答下列问题:
汽车是现代生活中不可缺少的工具之一.请回答下列问题:(1)汽车行驶过程中的能量来源是化学能
(2)汽车电路中的导线大都是铜制的,这是利用了金属铜的延展性和导电性.
(3)铝质承载式车身结构逐渐替代钢制,一部分原因是铁在潮湿的空气中容易锈蚀.喷漆可以延缓锈蚀,其防锈原理是隔绝氧气和水.
(4)在汽车尾气管上安装净化装置,可使尾气中的一氧化碳和一氧化氮气体在催化剂的表面发生反应,产生两种无毒的气体,分别是空气中含量最多的气体单质和气体化合物.该反应的化学方程式为2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2,反应前后氮元素的化合价分别为+2、0价.
分析 (1)根据汽车行驶过程中的能量转化进行分析解答;
(2)根据金属铜的延展性和导电性进行分析解答;
(3)根据铁的防锈原理进行分析解答;
(4)根据信息:CO与NO反应生成一种是空气中含量最多的气体可知是氮气,由质量守恒定律可知另一种氧化物是二氧化碳分析解答.
解答 解:(1)内燃机在促使汽车行驶中的能量转化过程是化学能转化为内能,再转化为机械能,故填:化学能;
(2)汽车电路中导线大都是铜的,利用的是铜的导电性和延展性,故填:导电;
(3)铁生锈是在氧气和水的共同作用下发生的;喷漆可以延缓锈蚀,其防锈原理是隔绝氧气和水;故填:氧气;
(4)CO与NO反应生成一种是空气中含量最多的气体可知是氮气,由质量守恒定律可知另一种氧化物是二氧化碳,反应的化学方程式为:2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2;一氧化氮中氧元素的化合价为-2价,所以氮元素的化合价为+2价,氮气中氮元素的化合价为0.
故填:2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2;+2、0价.
点评 本题主要考查合金的性质和化学方程式的书写等方面的知识,解答时应该根据质量守恒定律的内容正确的书写化学方程式,并且能够根据化合物中元素化合价代数和的特点求出某种元素的化合价.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
17.将50g食盐水恒温蒸发掉25g水(溶液仍未饱和),则溶液中的变化正确的是( )
| A. | 溶解度变大 | B. | 溶剂质量不变 | ||
| C. | 溶质质量不变 | D. | 溶质质量分数变大 |
15.下列事实解释不正确的是( )
| 事实 | 解释 | |
| A | 一氧化碳有毒性 | 一氧化碳分子有毒 |
| B | 钛合金可用来制人造骨骼 | 钛合金与人体有很好的相容性 |
| C | 水银体温计测量高烧病人的体温 | 原子间间隔受热时增大 |
| D | 金刚石、石墨的物理性质存在很大差异 | 碳原子的结构不同 |
| A. | A | B. | B | C. | C | D. | D |
16.下列说法正确的是( )
| A. | 氮气是由分子构成 | |
| B. | 当二氧化碳气体变成干冰,二氧化碳的分子间隙没有了 | |
| C. | 物质热胀冷缩是由分子的大小随温度发生改变 | |
| D. | 同种原子可以结合成分子,不同种原子不能结合成分子 |
 、
、 、
、 ”代表三种不同的原子,下图是某化学反应的微观模拟图,请根据图示回答下列问题.
”代表三种不同的原子,下图是某化学反应的微观模拟图,请根据图示回答下列问题.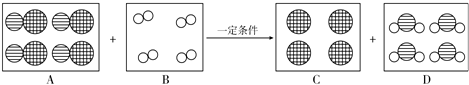
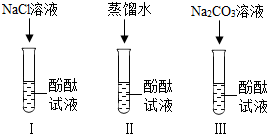 小宁和小明同学学习完酸、碱、盐后发现:碱溶液能使酚酞试液变红,Na2CO3溶液也能使酚酞试液变红.碱溶液使酚酞试液变红,是因为碱在水中解离出OH-,那么Na2CO3溶液中究竟是哪种粒子使酚酞试液变红呢?小宁设计了如图三个实验,请你、小宁和小明一起探究并完成下列问题:
小宁和小明同学学习完酸、碱、盐后发现:碱溶液能使酚酞试液变红,Na2CO3溶液也能使酚酞试液变红.碱溶液使酚酞试液变红,是因为碱在水中解离出OH-,那么Na2CO3溶液中究竟是哪种粒子使酚酞试液变红呢?小宁设计了如图三个实验,请你、小宁和小明一起探究并完成下列问题: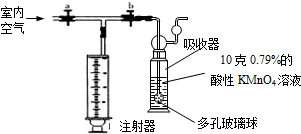 我国规定居室中装修材料释放出的甲醛气体含量不得超过0.08mg/m3.某研究小组通过查阅资料,拟采用“酸性高锰酸钾溶液褪色法”来测定居室中的甲醛气体含量.测定原理是:5X+4KMnO4+6H2SO4═2K2SO4+4MnSO4+5CO2↑+11H2O(X代表甲醛).操作过程为:用容积为1000mL的医用注射器抽取空气,缓慢注入酸性高锰酸钾溶液中(装置如下,a、b为止水夹),多次注气后当高锰酸钾溶液正好褪色时,停止注入.
我国规定居室中装修材料释放出的甲醛气体含量不得超过0.08mg/m3.某研究小组通过查阅资料,拟采用“酸性高锰酸钾溶液褪色法”来测定居室中的甲醛气体含量.测定原理是:5X+4KMnO4+6H2SO4═2K2SO4+4MnSO4+5CO2↑+11H2O(X代表甲醛).操作过程为:用容积为1000mL的医用注射器抽取空气,缓慢注入酸性高锰酸钾溶液中(装置如下,a、b为止水夹),多次注气后当高锰酸钾溶液正好褪色时,停止注入.