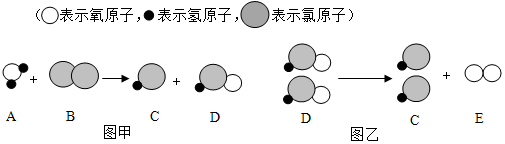
题目内容
2.从事科学实验的重要环节是进行科学实验设计.科学实验的正确步骤应为:①明确实验目的;②收集有关资料;③设计合理方案;④进行科学实验.请你按照以上四个步骤,完成以下实验设计,根据图回答问题: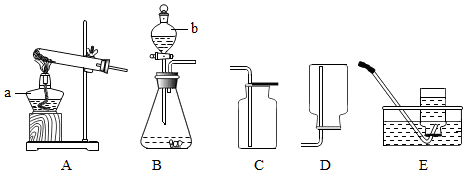
(1)写出仪器a、b的名称.a是酒精灯;b是分液漏斗.
(2)在实验室中用过氧化氢(H2O2)制取氧气.
【明确实验目的】用过氧化氢在实验室里制取氧气.
【收集有关资料】过氧化氢是一种无色液体,在二氧化锰的作用下,迅速分解出氧气,其反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
【设计合理方案】发生装置选用B(填序号,下同),收集装置选用C或E.
【进行科学实验】
(3)在实验室中,可以用加热氯酸钾(KClO3)和二氧化锰固体混合物制取氧气.
①【明确实验目的】.
②【收集有关资料】氯酸钾是白色的固体,二氧化锰是黑色的固体.且二氧化锰在反应中起作用.其反应的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
③【设计合理方案】发生装置选用,若选用C收集装置收集氧气,你验证集气瓶中是否已收集满的方法是把带火星的木条放在集气瓶口,木条复燃,证明集满.
(4)氢气是密度小于空气、难溶于水的气体,实验室用锌粒、稀硫酸混合制取氢气.制取氢气的发生装置应选择B,收集装置应选D或E.锌粒与稀硫酸反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)【收集有关资料】根据过氧化氢在二氧化锰的催化作用下分解生成水和氧气进行分析;
【设计合理方案】根据实验室用过氧化氢制取氧气的反应物是固体和液体,反应条件是常温,氧气不易溶于水,密度比空气大进行分析;
(3)②【收集有关资料】根据氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气进行分析;
③【设计合理方案】根据实验室用氯酸钾制取氧气的反应物是固体,反应条件是加热,氧气有助燃性进行分析;
(4)根据实验室制取氢气的反应物是固体和液体,反应条件是常温,氢气的密度比空气小,难溶于水,锌和硫酸反应生成硫酸锌和氢气进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,a是酒精灯,b是分液漏斗;
(2)【收集有关资料】过氧化氢在二氧化锰的催化作用下分解生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
【设计合理方案】实验室用过氧化氢制取氧气的反应物是固体和液体,反应条件是常温,氧气不易溶于水,密度比空气大,所以发生装置选用B,收集装置选用C或E;
(3)②【收集有关资料】氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
③【设计合理方案】实验室用氯酸钾制取氧气的反应物是固体,反应条件是加热,所以发生装置选用A,氧气有助燃性,所以验证集气瓶中是否已收集满的方法是:把带火星的木条放在集气瓶口,木条复燃,证明集满;
(4)实验室制取氢气的反应物是固体和液体,反应条件是常温,氢气的密度比空气小,难溶于水,锌和硫酸反应生成硫酸锌和氢气,所以制取氢气的发生装置应选择B,收集装置应选D或E,化学方程式为:Zn+H2SO4=ZnSO4+H2↑.
故答案为:(1)酒精灯,分液漏斗;
(2)【收集有关资料】2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
【设计合理方案】B,C或E;
(3)②【收集有关资料】2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
③【设计合理方案】A,把带火星的木条放在集气瓶口,木条复燃,证明集满;
(4)B,D或E,Zn+H2SO4=ZnSO4+H2↑.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

| A. | 只含碳氢两种元素 | |
| B. | 只有碳氢两种元素,可能含有氧元素 | |
| C. | 含有碳氢氧三种元素 | |
| D. | 含有碳氢两种元素,不含氧元素 |
| A. | 逐步淘汰高耗水生产工艺 | |
| B. | 农作物采用大水漫灌 | |
| C. | 生活污水集中处理后排放 | |
| D. | 工业“三废”经过处理达标后再排放. |