题目内容
工业上利用电石(CaC2)制备高纯碳酸钙的流程如下:
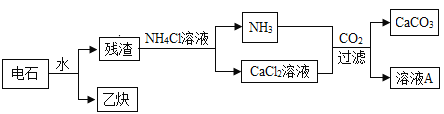
已知:①CaC2+2H2O=Ca(OH)2+C2H2↑;②CaCl2+H2O+CO2+2NH3=CaCO3↓+2NH4Cl。
(1)乙炔(C2H2)是一种常见的然料,当氧气不足时,除了生成水和二氧化碳外,还同时生成碳的另一种常见氧化物,写出乙炔不充分燃烧的化学方程式__________________。
(2)该流程中可循环使用的物质是______________(填名称)。
(3)电石长期露置于空气中,最终所得固体中一定含有碳酸钙,用化学方程式解释存在该物质的原因____________________。因此电石应该___________________保存。
某化学小组在老师的指导下对木炭还原氧化铜的实验进行探究,老师指出反应物之间的质量比不同可能会影响生成物的种类,在探究时,可以从定性观察和定量分析两个角度来判断生成物;请你跟随老师的思路,探究碳还原氧化铜生成的气体(假设所有反应均充分进行,浓硫酸能吸水,是常见的气体干燥剂)。
(提出问题)碳还原氧化铜生成的气体是什么?
(作出猜想)猜想①:CO;猜想②:CO2;猜想③:CO2和CO的混合物。
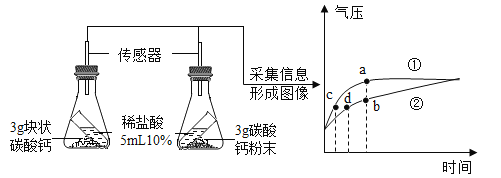
(实验设计)装置如图所示:
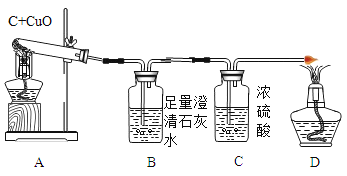
方案一:从定性观察角度判断:
(1)实验时,A中出现___________________的现象。
(2)若猜想①成立,B、D处会出现的现象是____________(填序号)。
aB中变浑浊,D处能点燃 bB中变浑浊,D处不能点燃
cB中无明显实验现象,D处能点燃 dB中无明显实验现象,D处不能点燃
方案二:从定量计算角度判断:
测定表格中的四个数据:
反应前的质量 | 反应后的质量 | |
A(试管+固体) | m1 | m2 |
B+C(广口瓶+溶液) | m3 | m4 |
(3)若猜想②成立,则m4-m3_________m1-m2 (选填“>”“<”或“=”),此时A中发生反应的化学方程式为______________________。
(4)若猜想③成立,且8gCuO全部参与反应,则生成的气体混合物的质量取值范围是__________________。


 五氧化二磷
五氧化二磷 氧化钙+二氧化碳
氧化钙+二氧化碳 B.过滤
B.过滤
 D.点燃酒精灯
D.点燃酒精灯
 质量多
质量多